Công thức electron của SO3 theo chương trình mới
1. Công thức electron của SO3
– Sự tạo thành phân tử SO3:
+ Nguyên tử sulfur (S) có cấu hình electron là 1s22s22p63s23p4 ⇒ S có 6 electron ở lớp ngoài cùng ⇒ Cần nhận thêm 2 electron để đạt được cấu hình electron bền vững giống khí hiếm.
+ Cấu hình electron của O là: 1s22s22p4 ⇒ O có 6 electron ở lớp ngoài cùng ⇒ Cần nhận thêm 2 electron để đạt được cấu hình electron bền vững của khí hiếm.
+ Nguyên tử S và một nguyên tử O sẽ góp chung 2 electron để tạo thành 2 cặp electron dùng chung. Khi đó nguyên tử S và một nguyên tử O đó đã đạt octet.
+ Còn hai nguyên tử O chưa đạt octet, S sẽ sử dụng một cặp electron chưa liên kết làm cặp electron chung với mỗi nguyên tử O còn lại. Nguyên tử S đóng góp cặp electron nên S là nguyên tử cho, còn nguyên tử O không đóng góp electron nên đóng vai trò nhận.
– Vậy công thức electron của SO3 là:
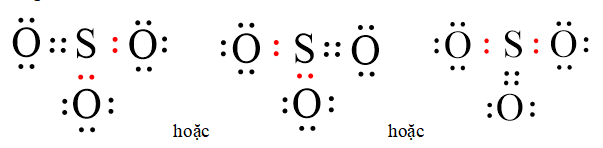
– Nhận xét:
+ Phân tử SO3 có 4 cặp electron chung, trong đó 2 cặp electron do một nguyên tử O và nguyên tử S góp chung, 2 cặp electron chỉ do nguyên tử S đóng góp.
+ Trong phân tử SO3 có 8 cặp electron tự do của các nguyên tử O, nguyên tử S không còn electron tự do.
2. Bài tập mở rộng về SO3
Câu 1. Công thức biểu diễn cấu trúc Lewis của phân tử SO3 là
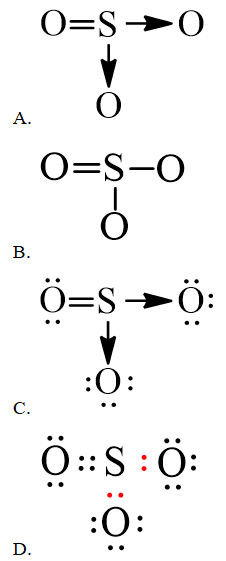
Hướng dẫn giải
Đáp án đúng là: C
Công thức Lewis của SO3 là:
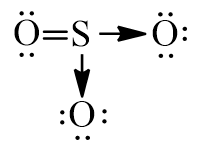
Đáp án A, B biểu diễn công thức cấu tạo của SO3
Đáp án D biểu diễn công thức electron của SO3.
Câu 2. Xét phân tử SO3, số cặp electron chỉ do nguyên tử S bỏ ra góp chung với các nguyên tử O thể hiện liên kết cho – nhận là
A. 1
B. 2
C. 3
D. 4
Hướng dẫn giải
Đáp án đúng là: B
Khi tạo thành phân tử SO3:
+ S và O cùng có 6 electron hóa trị và đều cần thêm 2 electron để đạt octet.
+ Nguyên tử S và một nguyên tử O sẽ góp chung 2 electron để tạo thành 2 cặp electron dùng chung. Khi đó nguyên tử S và một nguyên tử O đó đã đạt octet.
+ Còn hai nguyên tử O chưa đạt octet, S sẽ sử dụng một cặp electron chưa liên kết làm cặp electron chung với mỗi nguyên tử O còn lại. Nguyên tử S đóng góp cặp electron nên S là nguyên tử cho, còn nguyên tử O không đóng góp electron nên đóng vai trò nhận.
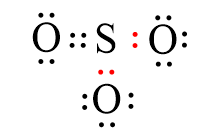
Vậy số cặp electron chỉ do nguyên tử S bỏ ra góp chung với các nguyên tử O thể hiện liên kết cho – nhận là 2.
Tham khảo các loạt bài Hóa học khác:
Công thức electron của SO3 theo chương trình mới
Công thức electron của HNO3 theo chương trình mới
Công thức electron của C2H2 theo chương trình mới
Công thức electron của C2H4 theo chương trình mới
Công thức electron của CS2 theo chương trình mới
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.





