Phản ứng: HCl + NaHSO4 → H2SO4 + NaCl
1. Phương trình phản ứng giữa NaHSO4 và HCl
HCl + NaHSO4 → H2SO4 + NaCl
2. Điều kiện xảy ra phản ứng
Nhiệt độ thường
3. Cách thức thực hiện phản ứng hóa học
Cho NaHSO4 tác dụng với dung dịch axit HCl.
4. Hiện tượng xảy ra sau khi phản ứng
Kết quả cuối cùng là tạo ra axit sulfuric (H2SO4) và muối clo (NaCl).
5. Bản chất của các chất tham gia phản ứng
5.1 Bản chất của HCl
HCl (axit clohidric) là một axit mạnh và có tính oxi hóa mạnh
5.2 Bản chất của NaHSO4
NaHSO4 hoạt động như một chất oxi hóa, cùng với HCl làm cho phản ứng trở nên khả thi.
6. Tính chất hóa học của HCl
Dung dịch axit HCl có đầy đủ tính chất hoá học của một axit mạnh.
6.1 Tác dụng chất chỉ thị:
Dung dịch HCl làm quì tím hoá đỏ (nhận biết axit)
HCl → H+ + Cl–
6.2 Tác dụng với kim loại
Tác dụng với KL (đứng trước H trong dãy Bêkêtôp) tạo muối (với hóa trị thấp của kim loại) và giải phóng khí hidrô (thể hiện tính oxi hóa)
Fe + 2HCl 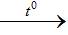 FeCl2 + H2
FeCl2 + H2
2Al + 6HCl 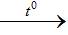 2AlCl3 + 3H2
2AlCl3 + 3H2
Cu + HCl → không có phản ứng
6.3 Tác dụng với oxit bazo và bazo:
Sản phẩm tạo muối và nước
NaOH + HCl → NaCl + H2 O
CuO + 2HCl 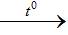 CuCl2 + H2 O
CuCl2 + H2 O
Fe2 O3 + 6HCl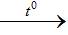 2FeCl3 + 3H2 O
2FeCl3 + 3H2 O
6.4 Tác dụng với muối (theo điều kiện phản ứng trao đổi)
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
AgNO3 + HCl → AgCl↓ + HNO3
(dùng để nhận biết gốc clorua )
Ngoài tính chất đặc trưng là axit , dung dịch axit HCl đặc còn thể hiện vai trò chất khử khi tác dụng chất oxi hoá mạnh như KMnO4, MnO2, K2 Cr2O7, MnO2, KClO3 ……
4HCl + MnO2 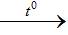 MnCl2 + Cl + 2H2 O
MnCl2 + Cl + 2H2 O
K2 Cr2 O7 + 14HCl → 3Cl2 + 2KCl + 2CrCl3 + 7H2 O
Hỗn hợp 3 thể tích HCl và 1 thể tích HNO3 đặc được gọi là hỗn hợp nước cường toan ( cường thuỷ) có khả năng hoà tan được Au ( vàng)
3HCl + HNO3 → 2Cl + NOCl + 2H2O
NOCl → NO + Cl
Au + 3Cl → AuCl3
7. Tính chất hóa học của NaHSO4
– NaHSO4 làm đổi màu quỳ tím sang đỏ
– NaHSO4 tác dụng với bazơ như NaOH, KOH, Ca(OH)2, Ba(OH)2
NaHSO4 + NaOH → Na2SO4 + H2O
NaHSO4 + Ba(OH)2 → BaSO4 + Na2SO4 + H2O
– Tác dụng với kim loại
NaHSO4 + Zn → ZnSO4 + Na2SO4 + H2
NaHSO4 + Na → Na2SO4 + H2
8. Tính chất hóa học của NaHSO4
Natri Hidro Sunfat là sản phẩm dạng hạt, khô rất dễ vận chuyển cũng như bảo quản. NaHSO4 là chất hút ẩm mạnh ở dạng khan. Dung dịch của muối này có tính axit mạnh. Nhiệt độ sôi và nhiệt độ nóng chảy cùng ở 315 độ C. Khối lượng mol của NaHSO4 nằm trong khoảng 120.06 g/mol, khối lượng riêng 2.742 g/cm3 .Đây là một hóa chất không tan trong amoniac nhưng lại phân hủy trong cồn.
9. Bài tập vận dụng liên quan
Câu 1:Phương trình ion rút gọn của phản ứng cho biết
A. Những ion nào tồn tại trong dung dịch.
B. Nồng độ những ion nào trong dung dịch lớn nhất.
C. Bản chất của phản ứng trong dung dịch các chất điện li.
D. Không tồn tại phân tử trong dung dịch các chất điện li.
Hướng dẫn giải:
Đáp án C
Phương trình ion rút gọn của phản ứng cho biết bản chất của phản ứng trong dung dịch các chất điện li.
Câu 2: Phản ứng nào sau đây là phản ứng trao đổi ion trong dung dịch các chất điện li?
A. 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
B. 2HCl + FeS → FeCl2 + H2S
C. NaOH + HCl → NaCl + H2O
D. Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Hướng dẫn giải:
Đáp án C
Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất một trong các chất sau: chất kết tủa, chất điện li yếu, chất khí.
Câu 3: Phương trình ion thu gọn: Ca2++CO32−→CaCO3↓ là của phản ứng xảy ra giữa cặp chất nào sau đây?
(1) CaCl2 + Na2CO3
(2) Ca(OH)2 + CO2
(3) Ca(HCO3)2 + NaOH
(4) Ca(NO3)2 + (NH4)2CO3
A. (1) và (2).
B. (2) và (3).
C. (1) và (4).
D. (2) và (4).
Hướng dẫn giải:
Đáp án C
(1), (4) có cùng phương trình ion thu gọn là Ca2++CO32−→CaCO3↓
(2) 2OH−+SO2→SO32−+H2O
(3) Ca2++HCO3−+OH−→CaCO3↓+H2O
Câu 4: Phản ứng nào dưới đây là phản ứng trao đổi ion trong dung dịch?
A. Zn + H2SO4 →ZnSO4 + H2
B. Fe(NO3)3 + 3NaOH → Fe(OH)3 + 3NaNO3
C. 2Fe(NO3)3 + 2KI → 2Fe(NO3)2 + I2 + 2KNO3
D. Zn + 2Fe(NO3)3 → Zn(NO3)2 + 2Fe(NO3)2
Hướng dẫn giải:
Đáp án B
A, C, D là phản ứng oxi hóa khử
B là phản ứng trao đổi ion trong dung dịch: Fe3++3OH−→Fe(OH)3↓
Câu 5: Phương trình H++OH−→H2O là phương trình ion thu gọn của phản ứng có phương trình sau:
A. NaOH + NaHCO3→ Na2CO3 + H2O
B. NaOH + HCl → NaCl + H2O
C. H2SO4 + BaCl2→ BaSO4 + 2HCl
D. 3HCl + Fe(OH)3→ FeCl3 + 3H2O
Hướng dẫn giải:
Đáp án B
Phản ứng có phương trình ion H++OH−→H2O
→ Phản ứng trung hòa axit với bazơ tan sinh ra muối tan và nước.
Câu 6:Cho phương trình phản ứng: KOH + HCl → KCl + H2O. Phương trình ion rút gọn của phản ứng trên là
A. H++OH−→H2O
B. K++Cl−→KCl
C. 2H++OH−→H2O
D.H++2OH−→H2O
Hướng dẫn giải:
Đáp án A
Phương trình ion thu gọn là: H++OH−→H2O
Câu 7: Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi:
A. các chất phản ứng phải là những chất dễ tan.
B. các chất phản ứng phải là những chất điện li mạnh.
C. một số ion trong dung dịch kết hợp được với nhau tạo thành chất kết tủa hoặc chất khí hoặc chất điện li yếu.
D. phản ứng không phải là thuận nghịch.
Hướng dẫn giải:
Đáp án C
Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất một trong các chất sau: chất kết tủa, chất điện li yếu, chất khí.
Câu 8: Cho 26,8 gam hỗn hợp X gồm CaCO3 và MgCO3 vào dung dịch HCl vừa đủ, thoát ra 6,72 lít khí (đktc) và dung dịch Y chứa m gam muối clorua. Giá trị của m là
A. 30,1.
B. 31,7.
C. 69,4.
D. 64,0.
Hướng dẫn giải:
Đáp án A
nCO2=0,3mol
Gọi số mol CaCO3 và MgCO3 trong hỗn hợp X lần lượt là x, y mol
Phương trình:
CaCO3 + 2H+→Ca2++CO2↑+H2O
BaCO3 + 2H+→Ba2++CO2↑+H2O
→100x+84y=26,8x+y=0,3→x=0,1y=0,2(mol)→m=0,1.111+0,2.95=30,1gam
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.




