1000 câu hỏi ôn tập Hóa (Phần 22)
Câu 1: Hòa tan một lượng sắt vào 500 ml dung dịch H2SO4 vừa đủ sau phản ứng thu được 33,6 lít khí H2 (ở đktc.)
a. Tính khối lượng của sắt tham gia phản ứng
b. Tính nồng độ mol của dung dịch H2SO4.
Lời giải:
nH2=33,622,4=1,5(mol)
PTHH: Fe + H2SO4 → FeSO4 + H2
Theo PTHH:
nH2=nFe=nH2SO4=1,5(mol)
a. mFe = 1,5.56 = 84 (g)
b.
⇒CMH2SO4=1,50,5=3M
Câu 2: Hòa tan 1,59 gam hỗn hợp A gồm kim loại M và Al trong lượng nước dư. Khuấy đều để phản ứng xảy ra hoàn toàn, có 0,04 mol khí hiđro thoát ra, còn lại 0,27 gam chất rắn không tan. M là kim loại nào?
A. Na;
B. K;
C. Ca;
D. Ba.
Lời giải:
Đáp án đúng là: B
Gọi hoá trị của kim loại M là n (
1≤n≤3
)
PTHH:
2M + 2nH2O → 2M(OH)n + nH2↑ (1)
2M(OH)n + 2nH2O + 2nAl → 2M(AlO2)n + 3nH2↑ (2)
Còn lại 0,27 gam chất rắn không tan là khối lượng Al dư, M tan hết
Gọi số mol của kim loại M là x (mol, x >0)
Theo PTHH (1):
nH2=n2nM=xn2(mol)
,
nM(OH)n=nM=x(mol)
Theo PTHH (2):
nH2=3n2nM(OH)n=3nx2(mol)
;
nAlpu=n.nM(OH)n=nx(mol)
Tổng số mol của H2 là:
4nx2=0,04⇒nx=0,02
(*)
Tổng hỗn hợp A là 1,59 gam →
MM.x+27.nx+0,27=1,59(**)
Thay (*) vào (**) ta được: MM.x = 0,78 (***)
Từ (*) ta có:
x=0,02n
thay vào (***), ta được:
MM.0,02n=0,78→MM=39n
Với n = 1 thì MM = 39 (g/mol)
Vậy M là kali (K).
Câu 3: Cho 10 gam CaCO3, MgCO3 vào 100 ml dung dịch HCl 1,5M, cho tới khi phản ứng xảy ra xong. Thể tích CO2 (đktc) thoát ra là:
A. 15,68 lít;
B. 1,68 lít;
C. 2,24 lít;
D. 2,88 lít.
Lời giải:
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
MgCO3 + 2HCl → MgCl2 + CO2↑ + H2O
Ta có:
10MMgCO3<nhh<10MCaCO3⇒0,1<nhh<0,12(mol)
→ 0,2 < nHCl = 2.nhh < 0,24
→ Hỗn hợp CaCO3 và MgCO3 dư, HCl phản ứng hết
nCO2=0,5nHCl=0,5.0,1.1,5 =0,075(mol)⇒VCO2=0,075.22,4=1,68(l)
Câu 4: Hòa tan hết 10,8 gam một oxit sắt vào dung dịch axit clohidric. Sau phản ứng thu đước 19,05 gam một muối sắt clorua. Hãy xác định công thức hóa học của oxit sắt?
Lời giải:
PTHH:
FexOy+ 2yHCl→xFeCl2yx+yH2O
Ta có:
19,05. (56x + 16y) = 10,8. (56x + 71y)
⇔
1066,8x + 304,8y = 604,8x + 766,8y
⇔
462x = 462y
⇔xy=11
Vậy CTHH của oxit sắt là FeO.
Câu 5: Hoà tan 100 ml HCl 1M vào 400 ml NaOH 1M thủ được dung dịch X. Tính pH của dung dịch X?
Lời giải:
HCl + NaOH → NaCl + H2O
nHCl = 0,1.1 = 0,1 (mol)
nNaOH = 0,4.1 = 0,4 (mol)
Vì HCl phản ứng với NaOH theo tỉ lệ 1:1 nên với lượng đề bài cho thì HCl phản ứng hết, NaOH còn dư
nNaOH dư = 0,4 – 0,1 = 0,3 (mol)
V = 100 + 400 = 500 (ml) = 0,5 lít
CMNaOH=0,30,5=0,6M→OH−=0,6M⇒pH=14+logOH−=13,77
Câu 6: Hòa tan hoàn toàn 10 gam hỗn hợp X gồm 2 muối khan FeSO4 và Fe2(SO4)3 vào nước. Dung dịch thu được phản ứng hoàn toàn với 1,58 gam KMnO4 trong môi trường axits H2SO4 dư. Thành phần phần trăm theo khối lượng của FeSO4 và Fe2(SO4)3 ban đầu lần lượt là:
A. 76% và 24%.
B. 67% và 33%.
C. 24% và 76%.
D. 33% và 67%.
Lời giải:
5Fe2++8H++MnO4−→5Fe3++Mn2++4H2OnFeSO4=5nKMnO4=5.1,58158=0,05(mol)⇒mFeSO4=0,05.152=7,6(g)⇒%mFeSO4=7,610.100%=76%
Câu 7: Hòa tan 14,2 gam P2O5 và m gam dung dịch H3PO4 35%, thu được dung dịch H3PO4 có nồng độ là 50%. Tính M.
Lời giải
P2O5 + 3H2O → 2H3PO4
142 → 2.98 = 196 (gam)
Coi P2O5 là dung dịch H3PO4 có:
Theo phương pháp đường chéo, ta có:
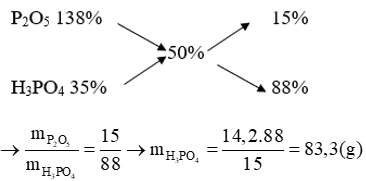
Câu 8: Hòa tan 14,88 g Na2O vào nước được dung dịch A. Cho 14,2 g P2O5 vào dung dịch A thu được dung dịch B. Cô cạn cẩn thận dung dịch B thu được bao nhiêu gam chất rắn
A. 78,72 g;
B. 30,16 g;
C. 29,72 g;
D. 24 g.
Lời giải
Đáp án đúng là: B
Ta có:
nNa2O=0,24nP2O5=0,1⇒nNaOH=0,48nH3PO4=0,2
→ Sinh ra muối Na2HPO4 và Na3PO4
Nhận thấy
nH2O=nNaOH=0,48(mol)
Bảo toàn khối lượng:
mH3PO4+mNaOH=mran+mH2O
→ 0,2.98 + 0,48.40 = mrắn + 0,48.18 → mrắn = 30,16 (g).
Câu 9: Hòa tan hoàn toàn 15,35 gam hỗn hợp kim loại gồm Mg, Al, Zn, Fe, Cu, Ag trong dung dịch HNO3 thu được 2,912 lít hỗn hợp khí NO, NO2, N2 có tỷ lệ mol 6:4:3 cô cạn cẩn thận dung dịch sau phản ứng thu được 82,15 gam muối. Số mol HNO3 phản ứng là?
A. 1,32;
B. 1,28;
C. 1,35;
D. 1,16.
Lời giải:
Đáp án đúng là: B
Số mol NO, NO2, N2 lần lượt là 0,06; 0,04; 0,03 mol
Giả sử chỉ tạo muối của các kim loại ta có:
mmuối = mkim loại +
mNO3−
tạo muối = 15,35 + 62.(0,06.3 + 0,04 + 0,03.10) = 47,59 g < 82,15g
⇒ mmuối = mkim loại + 62.(006.3+0,04+0,03.10+8.
nNH4NO3
+ 80.
nNH4NO3
⇒
nNH4NO3
= 0,06 mol
⇒ Sử dụng công thức tính nhanh
nHNO3=4nNO+2nNO2+12nN2+10nNH4NO3
= 4.0,06 + 2.0,04 + 12.0,03 + 10.0,06 = 1,28 mol
Câu 10: Hoà tan 17,5 gam hợp kim Zn, Fe, Al vào dung dịch HCl thu được V lít H2, đktc và dung dịch A. Cô cạn A thu được 31,7 gam hỗn hợp muối khan. Tính giá trị V.
Lời giải:
Gọi hỗn hợp 3 kim loại là X có hóa trị y, số mol HCl là a.
PTPƯ: 2X + 2yHCl → 2XCly + 2H2↑
Theo ĐLBTKL ta có:
mX+mHCl=mXCly+mH2
hay 17,5 + 36,5a = 31,7 + 2.0,5a
⇒ 17,5 + 36,5a = 31,7 + a
⇒ 36,5a – a = 31,7 − 17,5
⇒ 34,5a = 14,2
⇒
a=14,234,5=0,4(mol)
hay nHCl =0,4 mol
Theo phương trình:
nH2=12nHCl=0,2(mol)⇒VH2=0,2.22,4=4,48(l)
Câu 11: Hòa tan 28 gam Fe bằng dung dịch HCl 2M vừa đủ
a) Tính thể tích HCl cần dùng
c) Tính nồng độ mol của dung dịch thu được sau phản ứng (Coi thể tích dung dịch thu được sau phản ứng không thay đổi đáng kể so với thể tích ban đầu).
Lời giải:
a)
nFe=2856=0,5(mol)
Phương trình hoá học: Fe + 2HCl → FeCl2 + H2
Theo PTHH: nHCl = 2nFe = 2.0,5 = 1 (mol)
→VHCl=12=0,5(l)
b) Dung dịch thu được sau phản ứng: FeCl2
Theo phương trình hóa học :
nFeCl2=nFe=0,5(mol)
Vì thể tích dung dịch thu được sau phản ứng không thay đổi đáng kể
→Vdd thu được =VHCl =0,5 (l)
→
CMFeCl2=0,50,5=1(M)
Câu 12: Hoà tan 2,1 gam hỗn hợp X gồm Mg, Fe và Zn bằng một lượng vừa đủ dung dich HCl thấy thoát ra 1,12 lít khí H2 ở đktc.Tính lượng muối tạo thành?
Lời giải:
nH2=1,1222,4=0,05(mol)
nHCl=2nH2=2.0,05=0,1(mol)
Theo định luật bảo toàn khối lượng, ta có:
mmuối = 2,1 + 0,1.36,5 – 0,05.2 = 5,65 (g)
Câu 13: Hòa tan 2,4 gam CuO bằng 100 gam dung dịch H2SO4 29,4%
a) Tính khối lượng H2SO4 tham gia phản ứng
b) Tính C% các chất có trong dung dịch thu được.
Lời giải:
nCuO=2,480=0,03(mol)mH2SO4=100.29,4%=29,4(g)⇒nH2SO4=29,498=0,3(mol)
PTHH: CuO + H2SO4 → CuSO4 + H2O
nCuO<nH2SO4(0,03<0,3)
Nên CuO hết, H2SO4 dư
nH2SO4pu=nCuO=0,03(mol)⇒mH2SO4pu=0,03.98=2,94(g)nH2SO4du=0,3−0,03=0,27(mol)⇒mH2SO4du=0,27.98=26,46(g)mdd=mCuO+mddH2SO4=2,4+100=102,4(g)C%H2SO4=26,46102,4.100%=25,83%nCuSO4=nCuO=0,03(mol)⇒mCuSO4=0,03.160=4,8(g)C%CuSO4=4,8102,4.100%=4,6875%
Câu 14: Hoà tan 2,88 gam hỗn hợp gồm Ca, CaO, NaOH, KOH (trong đó số mol Ca bằng 1/6 số mol hỗn hợp) vào nước thu được dung dịch Z và 0,224 lít H2 đo đktc. Trung hoà dung dịch Z cần vừa đủ dung dịch HCl thu được dung dịch T. Cô cạn T thu được muối khan Q. Khối lượng của muối NaCl trong Q là:
A. 1,170;
B. 0,585;
C. 2,340;
D. 1,755.
Lời giải:
Đáp án đúng là: A
nCa=nH2=0,22422,4=0,01(mol)
→nhỗn hợp = 0,01.6 = 0,06 (mol)
Đặt nCaO + nKOH = a và nNaOH = b
→ a + b + 0,01 = 0,06 (1)
mhỗn hợp = 56a + 40b + 0,01.40 = 2,88 (2)
Giải (1) và (2), ta được: a = 0,03; b = 0,02
→ nNaCl = b = 0,02 (mol) → mNaCl = 1,17 (g).
Câu 15: Hòa tan hoàn toàn 2.81g hỗn hợp gồm Fe2O3, MgO, ZnO trong 500 ml H2SO4 0,1M vừa đủ sau phản ứng cô cạn dung dịch thu được m (g) hỗn hợp muối sunfat khan. Tính giá trị m?
Lời giải:
PTHH:
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
MgO + H2SO4 → MgSO4 + H2O
ZnO + H2SO4 → ZnSO4 + H2O
Theo các PTHH nhận thấy:
nH2O=nH2SO4=0,5.0,1=0,05(mol)
Áp dụng ĐL BTKL ta có:
moxit+mH2SO4=mmuoi+mH2O
→ m = mmuối = 2,81 + 0,05.98 − 0,05.18 = 6,81 (gam)
Câu 16: Hòa tan 20 gam hỗn hợp gồm Ag, Zn, Mg trong dung dịch H2SO4 0,5M thì có 6,72 lít khí ở đktc và còn lại 8,7 gam chất rắn không tan.
a) Xác định thành phần % theo khối lượng mỗi kim loại trong hỗn hợp
b) Tìm thể tích dung dịch H2SO4 đã dùng.
Lời giải:
a) Ta thấy 8,7 gam chất rắn không tan là Ag.
⇒ mZn,Mg = 20 – 8,7 = 11,3 (gam)
Đặt nMg = x(mol); nZn = y (mol) thì:
24x + 65y = 11,3 (1)
PTHH:
Mg + H2SO4 → MgSO4 + H2↑
x → x → x (mol)
Zn + H2SO4 → ZnSO4 + H2↑
y → y → y (mol)
Theo đề cho:
nH2
= 0,3 (mol)
⇒ x + y = 0,3 (2)
Từ (1) và (2) ta có hệ phương trình :
24x+65y=11,3x+y=0,3⇔x=0,2y=0,1
Do đó :
%mAg=8,9.100%20=44,5%%mMg=0,2.24.100%20=24%%mZn=100%−(44,5%+24%)=31,5%
b) Theo các PT:
nH2SO4
= x + y = 0,3 (mol)
⇒VH2SO4=0,30,5=0,6(l)
Câu 17: Hòa tan hoàn toàn 23 gam hỗn hợp gồm Ba và 2 kim loại kiềm A, B thuộc 2 chu kì liên tiếp vào nước thu được dung dịch D và 5,6 lít khí (đktc). Nếu thêm 0,09 mol Na2SO4 vào dung dịch D thì sau phản ứng vẫn còn dư ion Ba2+. Nếu thêm 0,105 mol Na2SO4 vào dung dịch D thì sau phản ứng còn dư Na2SO4. Tìm 2 kim loại kiềm.
Lời giải:
Đặt công thức chung của 2 kim loại kiềm A, B là R
PTHH:
Ba + 2H2O → Ba(OH)2 + H2
x x x (mol)
2R + 2H2O → 2ROH + H2
y y y/2 (mol)
Ba(OH)2 + Na2SO4 → BaSO4 + 2NaOH
x x
Theo bài ra ta có:
nH2
= x + y/2 = 0,25 (1)
mhh = 137x + MR.y = 23 (2)
0,09 < x < 0,105 (3)
Từ (1) và (2) →
x=0,5.MR−232MR−137
Kết hợp với (3) → 29,7 < R < 33,3
Mà 2 kim loại kiềm ở 2 chu kì liên tiếp nhau nên là Na và K.
Câu 18: Hòa tan 30g hỗn hợp Cu và CuO trong 1,5 lít dung dịch axit HNO3 1M (loãng) thấy thoát 6,72 lít NO (đktc) là sản phẩm khử duy nhất
1. Tính phần trăm khối lượng mỗi chất trong hỗn hợp ban đầu
2. Tính nồng độ mol của đồng (II) nitrat và dung dịch axit nitric sau phản ứng. Biết thể tích dung dịch sau phản ứng không thay đổi.
Lời giải:
nNO=6,7222,4=0,3(mol)
Sơ đồ phản ứng:
CuCu+2O0+HN+5O3→Cu+2(NO3)2+N+2O+H2O
Bảo toàn electron: 2nCu = 3nNO
→nCu=3.0,32=0,45(mol)
mCu = 0,45.64 = 28,8 (g)
%mCu=28,8.100%30=96%%mCuO=100%−96%=4%
b) Ta có:
mCuO = 30 – 28,8 = 1,2 (g)
→nCuO=1,280=0,015(mol)
Bảo toàn nguyên tố Cu:
nCu(NO3)2=nCu+nCuO=0,45+0,015=0,465(mol)→CMCu(NO3)2=0,4651,5=0,31M
Mặt khác:
nHNO3
ban đầu = 1,5.1 = 1,5 (mol)
Bảo toàn nguyên tố N:
nHNO3phanung=2nCu(NO3)2+nNO=2.0,465+0,3=1,23(mol)
⇒nHNO3du=1,5−1,23=0,27(mol)⇒CMHNO3=0,271,5=0,18M
Câu 19: Hòa tan 4,84 gam Mg kim loại bằng dung dịch HCl thấy thoát ra 0,4 gam H2
a) Xác định nguyên tử khối của Mg?
b) Mg kim loại ở trên có 2 đồng vị là
M1224g
và 1 đồng vị khác. Xác định số khối của đồng vị 2 biết tỉ số của hai loại đồng vị là 4:1.
Lời giải:
a) Mg + 2HCl → MgCl2 + H2 (1)
Theo (1)
nMg=nH2
= 0,4/2 = 0,2 mol
Suy ra MMg = 4,84/0,2 = 24,2 g/mol
b) Gọi đồng vị còn lại có số khối là
M12xg
vì tỉ số 2 đồng vị là 4:1 nên có 1 đồng vị chiếm 80%, 1 đồng vị chiếm 20%
TH1:
M1224g
chiếm 20% suy ra đồng vị còn lại chiếm 80%
Mtrung bình =24.20% + x.80% = 24,2 suy ra x = 24,25 (loại)
TH2:
M1224g
chiếm 80% suy ra đồng vị còn lại chiếm 20%
Mtrung bình=24.80% + x.20% = 24,2 suy ra x = 25
Vậy số khối của đồng vị còn lại là 25.
Câu 20: Hòa tan 4,9 mg H2SO4 vào nước thu dược 1 lít dung dịch. pH của dung dịch thu được là?
Lời giải:
nH2SO4=4,9.10−398=5.10−5(mol)⇒CMH2SO4=5.10−51=5.10−5(M)⇒H+=2.5.10−5=10−4M⇒pH=−logH+=4
Câu 21: Hoà tan 4 gam hỗn hợp Fe và một kim loại hoá trị II vào dung dịch HCl dư thu được 2,24 lít khí H2 (đktc). Nếu chỉ dùng 2,4 gam kim loại hoá trị 2 cho vào dung dịch HCl thì dùng không hết 500ml dung dịch HCl 1M. Tìm kim loại hoá trị II.
Lời giải:
Gọi kim loại là R
PTHH: Fe + 2HCl → FeCl2 + H2 (1)
R + 2HCl → RCl2 + H2 (2)
Theo PTHH (1), (2), ta có:
nH2=nFe+nR=2,2422,4=0,1(mol)
⇒Mhh=mhhnhh=40,1=40
Vì MFe = 56 > 40 → MR < 40
Mặt khác 2,4 gam R hoà tan thì dùng không hết 0,5 mol HCl
⇒nR<12nHCl=0,25(mol)⇒MR>2,40,25=9,6
Vậy 9,6 < MR < 40 → MR = 24 (g/mol)
Vậy R là magie (Mg).
Câu 22: Hòa tan 5,6 gam Fe bằng dung dịch HNO3 loãng (dư), sinh ra V lít khí NO (sản phẩm khử duy nhất, đktc). Giá trị của V là
A. 2,24;
B. 3,36;
C. 4,48;
D. 6,72.
Lời giải:
Đáp án đúng là: A
Bảo toàn số mol electron:
3nFe = 3nNO → nNO = nFe = 0,1 (mol) → VNO = 2,24 lít.
Câu 23: Hòa tan 5,4 gam một kim loại thuộc nhóm A bằng dung dịch HCl dư được 6,72 lít khí hiđro đktc. Tính kim loại đó?
Lời giải:
nH2=6,7222,4=0,3(mol)
– Gọi n là hóa trị của kim loại R cần tìm:
2R + 2nHCl → 2RCln + nH2
nR=2nnH2=0,6n(mol)
⇒MR=5,4n0,6=9n
n =1→ MR = 9 (loại)
n = 2 → MR = 18 (loại)
n = 3 → MR = 27 (Nhôm: Al)
Câu 24: Cho 6 gam hợp kim Cu, Fe và Al vào dung dịch axit HCl dư thấy thoát ra 3,024 lít H2 (đktc) và 1,86 gam chất rắn không tan. Thành phần phần trăm của hợp kim là
A. 40% Fe, 28% Al, 32% Cu;
B. 41% Fe, 29% Al, 30% Cu;
C. 42% Fe, 27% Al, 31% Cu;
D. 43% Fe, 26% Al, 31% Cu.
Lời giải
Đáp án đúng là: C
Vì Cu không tan trong HCl nên:
⇒mCu = 1,86 gam.
⇒mFe + mAl = 6 − 1,86 = 4,14 gam
nH2=3,02422,4=0,135(mol)
Gọi nFe là a (mol), nAl là b (mol).
PTHH: Fe + 2HCl → FeCl2 + H2↑ (1)
2Al + 6HCl → 2AlCl3 + 3H2↑ (2)
Theo đề bài ta có hệ
56a+27b=4,14a+1,5b=0,135⇒a=0,045b=0,06⇒%mCu=1,866.100%=31%%mFe=0,045.566.100%=42%%mAl=100%−31%−42%=27%
Câu 25: Hòa tan 7 gam một hỗn hợp 2 kim loại IIA (thuộc 2 chu kì liên tiếp) trong dung dịch HCl, thu 4,48 lít H2 (đktc).Tìm 2 kim loại đó?
Lời giải:
Gọi công thức chung của 2 kim loại là R
Phản ứng xảy ra:
R + 2HCl → RCl2 + H2
Ta có:
nH2=4,4822,4=0,2(mol)=nR⇒MR=70,2=35(g/mol)
Vì 24 < 35 < 40 và 2 kim loại nhóm IIA liên tiếp nhau nên 2 kim loại thỏa mãn là Mg; Ca.
Câu 26: Hòa tan hoàn toàn 8,5 gam hỗn hợp gồm 2 kim loại kiềm X, Y (ở 2 chu kì kế tiếp, MX<MY) vào nước thu được 3,36 lít khí H2 (ở đktc). Phần trăm khối lượng của X trong hỗn hợp ban đầu là
A. 72,95%.
B. 54,12%.
C. 27,05%.
D. 45,89%.
Lời giải:
Đáp án đúng là: B
nH2=3,3622,4=0,15(mol)
Gọi công thức chung của 2 kim loại kiềm là M
2M + 2H2O → 2MOH + H2↑
0,3 ← 0,15 (mol)
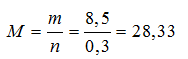
Þ Mx < 28,33 < MY và X, Y là 2 kim loại kiềm kế tiếp
Þ X là kim loại Na, Y là kim loại K.
Na: x ( mol) ; K: y (mol)
x+y=0,323x+39y=8,5⇒x=0,2y=0,1%mNa=0,2.238,5.100%=54,12%
Câu 27: Hoà tan 80 gam CuSO4 vào nước thu được 500 ml dung dịch
a) Tính
Cu2+
và
SO42−
trong dung dịch
b) Tính V dung dịch KOH 0,5M đủ để làm kết tủa hết ion
Cu2+
c) Tính V dung dịch BaCl2 0,25M đủ để làm kết tủa hết ion
SO42−
Lời giải:
nCuSO4=80160=0,5(mol)a,Cu2+=SO42−=0,50,5=1Mb,Cu2++2OH−→CuOH2
0,5……1 (mol)
⇒V=10,5=2(l)
c,
Ba2++SO42−→BaSO4
0,5……0,5 (mol)
⇒V=0,50,25=2(l)
Câu 28: Cho 9 gam hỗn hợp Mg và Al phản ứng hết với dung dịch HNO3 loãng thu được 6,72 lít khí không màu hoá nâu trong không khí là sản phẩm khử duy nhất và dung dịch X
a, Tính phần trăm khối lượng của các kim loại có trong hỗn hợp
b, Cho dung dịch KOH dư vào dung dịch X thì thu được bao nhiêu gam kết tủa?
Lời giải:
a, Đặt nMg = a; nAl = b
Ta có, hệ phương trình:
24a + 27b = 92a + 3b = 0,3.3⇒a=0,15b=0,2
Suy ra:
%mMg=0,15.249.100%=40%
, %mAl = 100% – 40% = 60%
b, Khi cho KOH dư thì Al(OH)3 sẽ tan tạo KAlO2
→ mkết tủa =
mMg(OH)2=0,15.58=8,7(g)
Câu 29: Hòa tan 9,4 gam K2O vào 190,6 gam H2O thu được A. Tính nồng độ % dung dịch A.
Lời giải:
Ta có phương trình hóa học
K2O + H2O → 2KOH
Áp dụng định luật bảo toàn khối lượng
→ mdung dịch KOH là 9,4 + 190,6 = 200 (g)
Ta có : mKOH = 0,2.(39 + 16 +1) = 11,2 gam
⇒C%=11,2200.100%=5,6%
Câu 30: Hoà tan hết 16,3 gam hỗn hợp kim loại gồm Mg, Al và Fe trong dung dịch H2SO4 đặc, nóng thu được 0,55 mol SO2. Cô cạn dung dịch sau phản ứng, khối lượng chất rắn khan thu được là?
Lời giải:
Bảo toàn electron:
2nMg+3nAl+3n=2nSO2=0,55.2=1,1(mol)
Muối thu được là: MgSO4, Al2(SO4)3, Fe2(SO4)3
Bảo toàn điện tích:
nSO42−=nMg2++32nAl3++32nFe3+=1,12=0,55(mol)
mmuối = mkim loại +
mSO42−
= 16,3 + 0,55.96 = 69,1 (g).
Câu 31: Hòa tan hết 37,725 gam hỗn hợp X gồm những lượng bằng nhau về số mol của NaHCO3, KHCO3, CaCl2, BaCl2 vào 130 ml nước cất, sau đó thêm tiếp 4,65 gam Na2O. Khuấy đều cho phản ứng xảy ra hoàn toàn, sau đó lọc bỏ kết tủa, thu được dung dịch Y. Tính nồng độ % của từng chất trong dung dịch Y. Giả thiết các kết tủa dạng khan và các chất không bị thất thoát trong quá trình thí nghiệm.
Lời giải:
Ta có:
nNa2O=4,6562=0,075(mol)
Gọi
nNaHCO3=nKHCO3=nCaCl2=nBaCl2=a(mol)
⇒mNaHCO3+mKHCO3+mCaCl2+mBaCl2=37,725
→ 84a + 100a + 111a + 208a = 37,725
→ a = 0,075
Các phản ứng xảy ra:
Na2O + H2O → 2NaOH
0,075………….0,15
NaHCO3 + NaOH → Na2CO3 + H2O
0,075…….0,075……0,075
2KHCO3 + 2NaOH → Na2CO3 + K2CO3 + 2H2O
0,075……..0,075…….0,0375…..0,0375
K2CO3 + BaCl2 → BaCO3 + 2KCl
0,0375…0,0375….0,0375….0,075
Na2CO3 + BaCl2 → BaCO3 + 2NaCl
0,0375…0,0375….0,0375…..0,075
Na2CO3 + CaCl2 → CaCO3 + 2NaCl
0,075……0,075……0,075…..0,15
Trong
YNaCl:0,225(mol)KCl:0,075(mol)
Xem
DH2O=1(g/ml)
Bảo toàn khối lượng:
mdd = 37,725 + 4,65 + 130.1 – 0,075.100 + 197.0,075 = 150,1 (g)
C%NaCl=0,225.58,5150,1.100%=8,77%C%KCl=0,075.74,5150,1.100%=3,72%
Câu 32: Hòa tan hết 6,3 gam hỗn hợp gồm Mg và Al trong vừa đủ 150 ml dung dịch gồm HCl 1M và H2SO4 1,5M thu được dung dịch X. Cô cạn dung dịch X thì thu được bao nhiêu gam muối khan?
A. 30,225 g
B. 33,225g
C. 35,25g
D. 37,25g
Lời giải:
Đáp án đúng là: B
150 ml = 0,15 (lít)
nHCl = V.CM HCl = 0,15.1 = 0,15 (mol)
nH2SO4
= V.CM = 0,15.1,5 = 0,225 (mol)
PTHH: Mg + 2HCl → MgCl2 + H2↑ (1)
2Al + 6HCl → 2AlCl3 + 3H2↑ (2)
Mg + H2SO4 → MgSO4 + H2↑ (3)
2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑ (4)
Theo PTHH (1) và (2) ta thấy:
nH2(1)+(2)=12nHCl=12.0,15=0,075(mol)
Theo PTHH (3) và (4) ta thấy:
nH2(3)+(4)=nH2SO4
= 0,225 (mol)
⟹ Tổng mol H2(1)+(2)+(3)+(4) = 0,075 + 0,225 = 0,3 (mol)
Bảo toàn khối lượng ta có:
mMg+Al + mHCl + mH2SO4 =mMgCl2 + mAlCl3 + mMgSO4 + mAl2SO43 + mH2
⟹ 6,3 + 0,15.36,5 + 0,225.98 = mmuối + 0,3.2
⟹ mmuối = 33,225 (g)
Câu 33: Hoà tan hết m gam ZnSO4 vào nước được dung dịch X. Cho 110 ml dung dịch KOH 2M vào X, thu được a gam kết tủa. Mặt khác, nếu cho 140 ml dung dịch KOH 2M vào X thì cũng thu được a gam kết tủa. Giá trị của m là
A. 20,125;
B. 22,54;
C. 12,375;
D. 17,71.
Lời giải:
Đáp án đúng là: A
Khi số mol KOH tăng mà vẫn thu được a gam kết tủa => Khi cho 0,22 mol KOH vào thì ZnSO4 còn dư => số mol kết tủa = 0,11 mol
Zn2+ + 2OH− → ZnOH2 ↓0,11…..0,22…….. 0,11
Khi cho 0,28 mol KOH thì ZnSO4 hết và số mol kết tủa vẫn còn là 0,11 mol:
ZnSO4 + 2OH– → Zn(OH)2 ↓
0,11+x 2(0,11+x) 0,11 + x
Zn(OH)2 + 2OH– →
ZnO22−
+ H2O
0,03 – x 0,06 – 2x
Theo giả thiết ta có: (0,11 + x) – (0,03 – x) = 0,11 => x = 0,015
Vậy số mol ZnSO4 ban đầu: 0,11 + 0,015 = 0,125 mol
=>
= 0,125.161 = 20,125 (g).
Câu 34: Hòa tan hoàn toàn 16,9 gam hỗn hợp gồm Mg, Fe, Zn bằng dung dịch HCl loãng, dư thì thu được 8,96 lít khí H2 (đktc) và dung dịch chứa m gam muối clorua. Giá trị m là
A. 45,3;
B. 55,3;
C. 46,1;
D. 56,1.
Lời giải:
Đáp án đúng là: A
Hỗn hợp gồm các kim loại khi tác dụng với dung dịch HCl loãng đều thể hiện hoá trị II nên gọi chung là R
PTHH: R + 2HCl → RCl2 + H2
Theo PTHH:
nHCl=2nH2=2.8,9622,4=0,8(mol)
Áp dụng định luật bảo toàn khối lượng, ta có:
mkim loại + mHCl = mmuối +
mH2
→ mmuối = 16,9 + 0,8.36,5 – 0,4.2 = 45,3 (g).
Câu 35: Tính nồng độ mol của ion hoà tan hoàn toàn 4,0 gam Fe2(SO4)3 vào 100 ml nước thu được dung dịch A.
Lời giải:
nFe2(SO4)3=4400=0,01(mol)Fe2SO43→2Fe3++3SO42−nFe3+=2nFe2(SO4)3=0,02(mol)nSO42−=3nFe2(SO4)3=0,03(mol)Fe3+=0,020,1=0,2MSO42−=0,030,1=0,3M
Câu 36: Hòa tan hoàn toàn 1,17 (g) một kim loại A có hoá trị không đối vào dung dịch HCI 1,2 (M) thì thu được 0,336 (1) khí. Tìm tên kim loại A và thế tích dung dịch HCI đã dùng.
Lời giải:
2A + 2nHCl → 2ACln + nH2
nH2=0,33622,4=0,015(mol)⇒nA=0,015.2n=0,03n(mol)⇒MA=1,170,03n=39n
→ n=1 thì MA = 39 (g/mol)
→ A là Kali (K)
nHCl=2nH2
= 0,015.2 = 0,03 (mol)
VHCl=0,031,2=0,025(l)=25(ml)
Câu 37: Hoà tan 10,4 gam hỗn hợp Mg, MgO cần vừa đủ a gam dung dịch H2SO4 loãng 9,8%, thu được 2,24 lít H2 (đkct) và 300 ml dung dịch A.
a, Tính % của mỗi chất trong hỗn hợp ban đầu.
b, Tính a, tính nồng độ mol chất tan trong dung dịch A và khối lượng riêng dung dịch.
Lời giải:
a) Mg + H2SO4 → MgSO4 + H2
MgO + H2SO4 → MgSO4 + H2O
nH2=V22,4=2,2422,4=0,1(mol)nMg=nH2=0,1(mol)
mMg = n.M = 0,1.24 = 2,4 (g)
%Mg=2,410,4.100%=23,08%%MgO=100%−23,08%=76,92%
b) mMgO = 10,4 − 2,4 = 8 (g)
nMgO=840=0,2(mol)nH2SO4=nMg+nMgO=0,1+0,2=0,3(mol)mH2SO4=n.M=0,3.98=29,4(g)mddH2SO4=29,4.1009,8=300(g)nMgSO4=nMg+nMgO=0,1+0,2=0,3(mol)CMMgSO4=nV=0,30,3=1Mmddspu=10,4+300−0,1.2=310,2(g)d=mV=310,2300=1,034(g/ml)
Câu 38: Hòa tan hoàn toàn 13,18 gam hỗn hợp X gồm Mg, và kim loại M (có hóa trị không đổi) bằng dung dịch chứa NaNO3 và HCl 0,76 mol, thu được dung dịch Y chỉ chứa muối và 1,792 lít hỗn hợp khí Z gồm 2 khí N2O và H2 có tỉ khối so với H2 là 14,125. Chia Y thành 2 phần bằng nhau. Đem cô cạn phần 1 thu được 21,64 g muối khan. Phần 2 cho tác dụng với KOH dư thu được 4,39 g kết tủa. Xác định kim loại M
Lời giải:
nZ=1,79222,4=0,08(mol);MZ=28,25
Áp dụng sơ đồ đường chéo, ta có:
N2O: 44 26,25
28,25
H2: 2 15,75
⇒nN2OnH2=26,2515,75=53⇒nN2O=0,05(mol);nH2=0,03(mol)
m↓ = 4,93.2 = 9,86 < mX = 13,18
mmuối = 21,64.2 = 43,28 (g)
Giả sử dung dịch Y không chứa muối amoni
nNa+=nNO3−=2nN2O=0,1(mol)⇒mY=mNa++mX+mCl−=0,1.23+13,18+0,76.35,5=42,46<43,28
→ Dung dịch Y chứa muối
NH4+
( x mol)
Y gồm:
Mg2+(0,15mol);NH4+(xmol);Cl−(0,76mol);Na+(x+0,1mol);Mn+
mY = 13,18 + 18x + 35,5.0,76 + 23.(0,1 + x) = 43,28 → x = 0,02
mM = mX – mMg = 13,18 – 0,17.24 = 9,1
Bảo toàn electron:
n.nM+2nMg=8nNH4++8nN2O+2nH2=8.0,02+8.0,05+2.0,03=0,62⇒9,1MM.n=0,62−2.0,17=0,28⇒MM=32,5n⇒n=2MM=65
Vậy M là kẽm (Zn).
Câu 39: Hòa tan hoàn toàn 13,45 gam hỗn hợp 2 muối hidro cacbonat và cacbonat trung của 1 kim loại kiềm bằng 300 ml dung dịch HCl 1M. Sau phản ứng phải trung hòa HCl dư bằng 75 ml dung dịch Ca(OH)2 1M. Công thức 2 muối:
A. KHCO3, K2CO3
B. NaHCO3, Na2CO3
C. LiHCO3, Li2CO3
D. Cả A, B đều đúng.
Lời giải:
Đáp án đúng là: A
nHCl = 0,3 mol
nCa(OH)2
= 0,075 mol
AHCO3 + HCl → ACl + CO2 + H2O
x x
A2CO3 + 2HCl → 2ACl + CO2 + H2O
y 2y
Ca(OH)2 + 2HCl → CaCl2 + 2H2O
0,075 0,15
Ta có: x + 2y = 0,15
Với 0 < y < 0,075
Mặt khác: Ax + 61x + 2Ay +60y = 13,45
Þ A.(0,15 – 2y) + 61.(0,15 – 2y) + 2Ay + 60y = 13,45
Þ 0,15A – 2Ay + 9,15 – 122y + 2Ay + 60y = 13,45
Þ 0,15A – 4,3 = 62y
Þ
y=15A−4,362
Với y > 0 Þ
15A−4,362>0
Þ A > 28,7 (1)
Với y < 0,075 Þ
15A−4,362<0,075
Þ A< 59,7 (2)
Từ (1) và (2): 28,7 < A < 59,7
Þ A là kali
Þ CTHH: KHCO3, K2CO3
Câu 40: Hòa tan hoàn toàn 14,5 gam hỗn hợp gồm Mg, Fe, Zn bằng dung dịch HCl dư thì thu được 6,72 lít khí H2 (đktc) và dung dịch chứa m gam muối clorua. Tính m. A. m = 35,8 (g);
B. m = 25,45 (g);
C. m = 24,85 (g);
D. m = 36,4 (g).
Lời giải:
Đáp án đúng là: A
Hỗn hợp gồm các kim loại khi tác dụng với dung dịch HCl loãng đều thể hiện hoá trị II nên gọi chung là R
PTHH: R + 2HCl → RCl2 + H2
Theo PTHH:
nHCl=2nH2=2.6,7222,4=0,6(mol)
Áp dụng định luật bảo toàn khối lượng, ta có:
mkim loại + mHCl = mmuối +
mH2
→ mmuối = 14,5 + 0,6.36,5 – 0,3.2 = 35,8 (g).
Câu 41: Hòa tan hoàn toàn 15,9g hỗn hợp 3 kim loại Al, Mg, Cu bằng dd HNO3 thu được 6,72 lit khí NO (là sản phẩm khử duy nhất ở đktc) và dd X. Đem cô cạn dd X thì thu được khối lượng muối khan là
A. 77,1 g;
B. 71,7 g;
C. 17,7 g;
D. 53,1 g.
Lời giải:
Đáp án đúng là: B
Ta có:
nNO3−
(muối) = ne nhường = ne nhận = 3nNO = 0,9 mol
mmuối = mkim loại +
mNO3−
= 15,9 + 0,9.62 = 71,7 (g)
Câu 42: Hòa tan hoàn toàn 2,16 gam Al bằng một lượng vừa đủ dung dịch H2SO4 20%. Sau phản ứng thu được dung dịch X và khí H2
a. Tính khối lượng muối tạo thành trong dung dịch X.
b. Tính khối lượng dung dịch X thu được sau phản ứng.
Lời giải:
a)
nAl=2,1627=0,08(mol)
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
0,08………………0,04 mol
X: Al2(SO4)3
mX=mAl2(SO4)3=0,04.342=13,68(g)
b) Theo PTHH có:
nH2=nH2SO4=32nAl=32.0,08=0,12(mol).
Khối lượng dung dịch H2SO4 20% là:
mdd H2SO4 20%=0,12.9820.100=58,8 gam.
Bảo toàn khối lượng:
mAl+mdd H2SO4 20%=mddX+mH2
Þ mdd X = 2,16 + 58,8 – 0,12.2 = 60,72 gam.
Câu 43: Hòa tan hoàn toàn 2,16 gam Al trong dung dịch HNO3 1M thu được 1,232 lít hỗn hợp B gồm NO và N2O (đktc). Tính tỷ khối của B so với H2?
Lời giải:
nAl=2,1627=0,08(mol)nhh=nNO+nN2O =1,23222,4=0,055(mol)
Gọi
nNO:a(mol)nN2O:b(mol)⇒a+b=0,0553a+8b=0,08.3⇒a=0,04b=0,015MB¯=0,04.30+0,015.440,055=37211⇒dB/H2=18611
Câu 44: Hòa tan hoàn toàn 2,4 gam kim loại Mg vào dung dịch HNO3 loãng, giả sử chỉ thu được V lít khí N2 là sản phẩm khử duy nhất (đktc). Giá trị của V là:
A. 0,672 lít;
B. 6,72 lít;
C. 0,448 lít;
D. 4,48 lít.
Lời giải:
Đáp án đúng là: C
nMg = 0,1 (mol)
Ta có các quá trình:
Mg0→Mg+2+2e0,1……………0,2 2N+5+10e→N20⇒nN2=0,210=0,02(mol)⇒VN2=0,02.22,4=0,448(l)
Câu 45: Hòa tan hoàn toàn 2 gam kim loại R hóa trị II vào m gam dung dịch HCl 10% thu được 1,2395 lít khí (đkc) và dung dịch A.
a. Xác định tên kim loại R.
b. Để trung hoà lượng HCl dư trong dung dịch A cần dùng 100 ml dung dịch NaOH 2M. Tính m.
Lời giải:
a) R + 2HCl → RCl2 + H2
nH2=1,239524,79=0,05(mol)
Theo PTHH:
nR=nH2=0,05(mol)
⇒MR=20,05=40(g/mol)
Vậy R là canxi (Ca).
b)
nHCl=2nH2=0,1(mol)
100 (ml) = 0,1 (l)
nNaOH = 0,1.2 = 0,2 (mol)
HCl + NaOH → NaCl + H2O
Theo PTHH: nHCl (dư) = nNaOH = 0,2 (mol)
Tổng số mol HCl ban đầu là: 0,1 + 0,2 = 0,3 (mol)
⇒mddHCl=0,3.36,510%=109,5(g)
Câu 46: Hòa tan hoàn toàn 2,43 gam hỗn hợp gồm Mg và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng, sau phản ứng thu được 1,12 lít H2 (đktc) và dung dịch X. Khối lượng muối trong dung dịch X là
A. 5,83 gam.
B. 4,83 gam.
C. 7,33 gam.
D. 7,23 gam.
Lời giải:
Đáp án đúng là: D
Ta có mMuối = mKim loại +
mSO42−
Mà
nSO42−=nH2
= 0,05 mol.
⇒ mMuối = 2,43 + 0,05×96 = 7,23 gam.
Câu 47: Hòa tan hoàn toàn 4,88 gam hỗn hợp X gồm FexOy và Cu trong lượng dư dung dịch H2SO4 đặc nóng. Thu được 1,008 lít khí SO2 sản phẩm khí duy nhất ở điều kiện tiêu chuẩn và dung dịch chứa 13,2 gam hỗn hợp 2 muối sunfat. Tìm công thức oxit sắt và tính khối lượng của mỗi chất có trong hỗn hợp X.
Lời giải:
nSO2=1,00822,4=0,045(mol)
Quy đổi hỗn hợp thành Fe (a mol), Cu (b mol) và O (c mol)
→mX = 56a + 64b + 16c = 4,88 (1)
Bảo toàn electron: 3a + 2b = 2c + 2
nSO2
= 2c + 0,09 (2)
Muối gồm Fe2(SO4)3 (0,5a mol) và CuSO4 (b mol)
mmuối = 400.0,5a + 160b = 13,2 (3)
Giải (1), (2), (3), ta được: a = 0,05; b = 0,02; c = 0,05
→ Fe : O = a : c = 1 : 1 → FeO
X gồm FeO (0,05 mol) và Cu (0,02 mol)
Khối lượng của mỗi chất có trong hỗn hợp X là:
mFeO = 0,05.72 = 3,6 (g); mCu = 0,02.64 = 1,28 (g)
Câu 48: Hoà tan hết 7,74 gam hỗn hợp bột Mg, Al bằng 500 ml dung dịch hỗn hợp HCl 1M và H2SO4 0,28M thu được dung dịch X và 8,736 lít khí H2 (ở đktc). Cô cạn dung dịch X thu được lượng muối khan là:
A. 38,93 gam;
B. 103,85 gam;
C. 25,95 gam;
D. 77,86 gam.
Lời giải:
Đáp án đúng là: A
Số mol của hiđro bằng:
nH2=8,73622,4=0,39(mol)
Lại có:
nHCl=5001000.1=0,5(mol);nH2SO4=5001000.0,28=0,39(mol)
Khối lượng muối tạo thành bằng: 7,74 + 0,5.36,5 + 0,14.98 – 0,39.2 = 38,93 (gam).
Câu 49: Hòa tan hoàn toàn 7,83 gam hỗn hợp X gồm hai kim loại đều hóa trị I vào 100 gam dung dịch HCl 3,65%, sau phản ứng thu được dung dịch Y. Để trung hoà hoàn toàn Y cần 150 ml dung dịch HNO3 1M. Tính khối lượng chất rắn khan khi cô cạn Y và tìm hai kim loại trong X.
Lời giải:
nHCl=100.3,65%36,5=0,1(mol);nHNO3=0,15(mol)
X gồm cation kim loại (7,83 gam), Cl– (0,1 mol), OH– (0,15 mol)
→ mrắn = 13,93 gam
nX = nHCl +
nHNO3
= 0,25 (mol)
→ MX = 31,32
Nếu 2 kim loại kế tiếp thì X gồm Na, K.
Câu 50: Hòa tan hoàn toàn 9,6 gam hỗn hợp A gồm Fe và kim loại R thuộc nhóm IIA (có hóa trị II) vào dung dịch HCl dư thu được 4,48 lít khí không màu (đktc). Mặt khác khi hòa tan hoàn toàn 4,6 gam kim loại R trong 500ml dung dịch HCl 1M thì thu được dung dịch B. Cho quỳ tím vào dung dịch B thấy quỳ tím chuyển thành màu đỏ. Xác định kim loại R. Tính% khối lượng mỗi kim loại trong hỗn hợp A.
Lời giải:
– Nếu R là Mg: %mFe = 87,5%; %mMg = 12,5%
– Nếu R là Ca: %mFe =58,33%; %mCa = 41,63%
Giải thích các bước giải:
Gọi số mol Fe và R là a và b
Ta có: 56a + R.b = 9,6 (1)
nH2=4,4822,4=0,2(mol)
Phương trình hóa học:
Fe + 2HCl → FeCl2 + H2
R + 2HCl → RCl2 + H2
Ta có: a + b = 0,2 (2)
Vì khi cho quỳ vào thì hóa đỏ, nên HCl còn dư
→nHCl phản ứng < nHCl = 0,5 mol
→nR=nHCl2=0,52=0,25(mol)
→R>4,60,25=18,4
Từ (1) và (2) ta có:
R=9,6−56a0,2−a=56−1,60,2−a<56
→18,4 < R < 56
→R là Mg hoặc Ca
– Nếu R là Mg
a + b =0,2 và 56a + 24b = 9,6
→a = 0,15; b = 0,05
→%mFe=0,15.569,6.100%=87,5%
→%mMg = 12,5%
– Nếu R là Ca
a + b = 0,2 và 56a + 40b = 9,6
→a = b = 0,1
→%mFe=0,1.569,6.100%=58,33%
→%mCa = 41,63%.
Xem thêm các câu hỏi ôn tập Hóa học chọn lọc, hay khác:
1000 câu hỏi ôn tập môn Hóa có đáp án (Phần 18)
1000 câu hỏi ôn tập môn Hóa có đáp án (Phần 19)
1000 câu hỏi ôn tập môn Hóa có đáp án (Phần 20)
1000 câu hỏi ôn tập môn Hóa có đáp án (Phần 21)
1000 câu hỏi ôn tập môn Hóa có đáp án (Phần 23)
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.





