Phản ứng CuSO4 + Na2S → CuS + Na2SO4
1. Phương trình phản ứng CuSO4 tác dụng Na2S
CuSO4 + Na2S → CuS↓ + Na2SO4
2. Phương trình ion rút gọn CuSO4 + Na2S
Cu2+ + S2− → CuS↓
3. Hiện tượng CuSO4 tác dụng Na2S
Xuất hiện kết tủa đen Đồng II sunfua (CuS) trong dung dịch.
4. Mở rộng kiến thức về CuSO4
4.1. Tính chất vật lí và nhận biết
– Tính chất vật lí: Đồng (II) sulfat CuSO4 là chất bột màu trắng, hút mạnh hơi ẩm của không khí để tạo thành hiđrat CuSO4.5H2O màu lam. Lợi dụng tính chất này, người ta dùng CuSO4 khan để phát hiện nước ở lẫn trong hợp chất hữu cơ.
– Tan tốt trong nước.
– Nhận biết: Khi có mặt nước, CuSO4 tan dần, chuyển từ chất bột màu trắng sang dung dịch có màu xanh.
4.2. Tính chất hóa học
Có tính chất hóa học của muối.
– Tác dụng với dung dịch bazo:
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
CuSO4 + Ba(OH)2 → Cu(OH)2 + BaSO4
– Tác dụng với muối:
BaCl2 + CuSO4 → CuCl2 + BaSO4
4.3. Điều chế
– Cho đồng (II) oxit tác dụng với H2SO4
CuO + H2SO4 → CuSO4 + H2
– Cho đồng phản ứng với H4SO4 đặc nóng
Cu + 2H2SO4 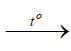 CuSO4 + SO2 +2H2O
CuSO4 + SO2 +2H2O
4.4. Ứng dụng
– CuSO4 ứng dụng trong nông nghiệp.
Đồng Sunphat được sử dụng làm nguyên liệu trong phân bón để làm tăng sức đề kháng cũng như chống chọi được sâu bệnh cho cây trồng. Đồng thời, bổ sung vi lượng Cu khi cây bị thiếu.
Đồng sunphat được sử dụng như là thuốc kháng nấm hoặc làm thuốc diệt các loại sâu bệnh, diệt cỏ.
Đồng sunphat được bổ sung vào cây trồng để tác động đến sự tổng hợp của các chất như đường bột, đạm, chất béo, enzim.
Đồng sunphat là một thành phần trong nguyên liệu cho thức ăn chăn nuôi để bổ sung đồng cho vật nuôi và được xem là chất điều hòa sinh trưởng.
– CuSO4 ứng dụng trong phòng thí nghiệm.
Đồng sulfat được dùng làm thuốc thử trong một số thí nghiệm ví dụ:
Đồng sulfat được sử dụng trong dung dịch Fehling và dung dịch của Benedict để kiểm tra các đường làm giảm , làm giảm sulfat đồng màu xanh hòa tan (II) thành oxit đồng đỏ không hòa tan (I).
Đồng sulfat dùng để kiểm tra ngọn lửa, các ion đồng của nó phát ra ánh sáng màu lục sâu, màu xanh sâu hơn nhiều so với kiểm tra ngọn lửa cho barium .
Đồng sulfat còn được dùng để xét nghiệm máu để xác định tình trạng của máu. Máu được thử nghiệm bằng cách thả nó vào dung dịch của đồng sulfat có trọng lượng riêng – máu chứa đầy đủ hemoglobin bồn chứa nhanh chóng do mật độ của nó, trong khi máu không chìm hoặc chìm từ từ không có đủ lượng hemoglobin .
– CuSO4 ứng dụng trong các ngành công nghiệp khai thác và sản xuất.
Đồng sunphat dùng để điều chế các chất xúc tác sử dụng trong chế biến, khai thác dầu khí và chất lỏng
– Đồng sunphat còn được ứng dụng trong ngành dệt may hoặc dùng trong thuốc nhuộm vải để tăng độ bền của thuốc nhuộm.
– Đồng sunphat trong công nghệ thực phẩm được sử dụng như chất tạo màu cho thực phẩm. Thành phần của dung dịch sử dụng để bảo quản mẫu vật thực vật có màu sắc tự nhiên và ngăn ngừa sự thối rữa của trái cây.
Đồng sunphat dùng là chất tạo màu trong công nghệ pháo hoa hoặc in ấn, làm kính và đồ gốm.
-Đồng sunphat trong ngành công nghiệp sơn sử dụng như là chất sơn chống bẩn.
5. Tính chất hoá học của Na2S
– Phản ứng với thuốc thử vô cơ
S2- + H2O → HS– + OH–
– Phản ứng oxy hóa khi tiến hành đun nóng Na2S với natri cacbonat với lưu huỳnh dioxit
2Na2S + 3O2 + 2CO2 → 2Na2CO3 + 2SO2
– Phản ứng oxy hóa cùng với hidro peroxit
Na2S + 4H2O2 → 4H2O + Na2SO4
– Cho lưu huỳnh phản ứng với natri sunfua tạo thành polysulfides
2Na2S + 8S → 2Na2S5
– Natri sunfua + HCl sinh ra H2S – một loại khí độc với mùi hôi thối
Na2S + 2HCl → 2NaCl + H2S
6. Bài tập vận dụng liên quan
Câu 1. Trường hợp xảy ra phản ứng là
A. Cu + Pb(NO3)2.
B. Cu + HCl loãng
C. Cu + HCl + O2.
D. Cu + H2SO4 loãng.
Lời giải:
Câu 2. Cho m gam Cu phản ứng hết với dung dịch HNO3 thu được 4,48 lít (đktc) hỗn hợp khí NO và NO2 có khối lượng là 7,6 gam. Giá trị của m là
A. 25,6
B. 16.
C. 2,56.
D. 12,8.
Lời giải:
Câu 3. Cho các kim loại: Cu, Al, Fe, Au, Ag. Dãy gồm các kim loại được sắp xếp theo chiều tăng dần tính dẫn điện (từ trái sang phải) là
A. Fe < Au < Al < Cu < Ag
B. Fe < Al < Au < Cu < Ag
C. Fe < Al < Cu < Ag < Au
D. Al < Fe < Au < Cu
Lời giải:
Câu 4. Cho các kim loại: Cu, Al, Fe, Au, Zn. Số kim loại phản ứng được với dung dịch HCl là:
A. 2
B. 3
C. 5
D. 4
Lời giải:
Xem thêm các phương trình hóa học khác:
Cu + HNO3 → Cu(NO3)2 + NO2 + H2O
Cu + HNO3 → Cu(NO3)2 + N2O + H2O
Cu + HNO3 → Cu(NO3)2 + NO+ H2O
Cu+ H2SO4 → CuSO4 + SO2 + H2O
Cu + AgNO3 → Cu(NO3)2 + Ag
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.




