Phản ứng K + FeCl2 + H2O → KCl + H2 + Fe(OH)2
1. Phản ứng hóa học
2K + FeCl2 + 2H2O → 2KCl + H2 + Fe(OH)2
2. Điều kiện phản ứng
Không cần điều kiện
3. Cách thực hiện phản ứng
Cho kali tác dụng với dung dịch muối sắt (II) clorua
4. Hiện tượng nhận biết phản ứng
Kali tan dần trong dung dịch muối sắt (II) clorua, có kết tủa màu trắng xanh tạo thành và có khí thoát ra.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của K (Kali)
– Trong phản ứng trên K là chất khử.
– K là chất khử mạnh, K tham gia phản ứng với các dung dịch muối sẽ tham gia phản ứng với nước trước tạo hidroxit và giải phóng H2.
5.2. Bản chất của FeCl2 (Sắt (II) clorua)
FeCl2 mang tính chất hoá học của muối tác dụng được với dung dịch kiềm.
6. Tính chất hoá học của K
Kali là kim loại kiềm có tính khử rất mạnh.
K → K+ + 1e
6.1. Tác dụng với phi kim
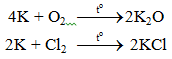
6.2. Tác dụng với axit
2K + 2HCl → 2KCl + H2.
6.3. Tác dụng với nước
K tác dụng mãnh liệt với nước và tự bùng cháy tạo thành dung dịch kiềm và giải phóng khí hidro.
2K + 2H2O → 2KOH + H2.
6.4. Tác dụng với hidro
Kali tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 – 400oC tạo thành kali hidrua.
2K (lỏng) + H2 (khí) → 2KH (rắn)
7. Mở rộng kiến thức về FeCl2
7.1. Tính chất vật lí và nhận biết
– Tính chất vật lý: Nó là một chất rắn thuận từ có nhiệt độ nóng chảy cao, và thường thu được dưới dạng chất rắn màu trắng. Tinh thể dạng khan có màu trắng hoặc xám; dạng ngậm nước FeCl2.4H2O có màu xanh nhạt. Trong không khí, dễ bị chảy rữa và bị oxi hoá thành sắt (III).
– Nhận biết: Sử dụng dung dịch AgNO3, thấy xuất hiện kết tủa trắng.
FeCl2 + 2AgNO3 → Fe(NO3)2 + 2AgCl↓
7.2. Tính chất hóa học
– Mang đầy đủ tính chất hóa học của muối.
– Có tính khử Fe2+ → Fe3+ + 1e
a) Tính chất hóa học của muối:
– Tác dụng với dung dịch kiềm:
FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
– Tác dụng với muối
FeCl2 + 2AgNO3 → Fe(NO3)2 + 2AgCl
b) Tính khử:
Thể hiện tính khử khi tác dụng với các chất oxi hóa mạnh:
2FeCl2 + Cl2 → 2FeCl3
7.3. Điều chế
– Cho kim loại Fe tác dụng với axit HCl:
Fe + 2HCl → FeCl2 + H2
– Cho sắt (II) oxit tác dụng với HCl
FeO + 2HCl → FeCl2 + H2O
7.4. Ứng dụng
– FECL2 ở dạng dung dịch 30% sẽ có các công dụng sau đây:
Công dụng nổi bật nhất của dung dịch Sắt II Clorua này chính là để làm hóa chất xử lý nước thải trong nhiều ngành công nghiệp sản xuất như nước thải ngành dệt nhuộm, ngành chăn nuôi, ngành xi mạ, nước thải của bệnh viện, …
– FeCl2 ở dạng khác còn ứng dụng với các mục đích sau:
FECL2 có mặt trong nông nghiệp thông qua việc là một trong những chất phụ gia sử dụng trong sản xuất thuốc trừ sâu.
FECL2 đối với công nghiệp nhuộm vải và ngành dệt thì có công dụng là một trong những chất cầm màu rất hiệu quả.
FECL2 ứng dụng trong phòng thí nghiệm.
– Dùng trong phòng thí nghiệm hoá học và điều chế sắt (III) clorua.
8. Câu hỏi vận dụng
Câu 1. Khi cho K tác dụng với dung dịch muối sắt (II) clorua. Phương trình phản ứng xảy ra là:
A. 2K + FeCl2 + 2H2O → 2KCl + H2 + Fe(OH)2
B. 2K + 2FeCl2 → KCl + FeCl3 + Fe
C. 2K + FeCl2 + 2H2O → 2KCl + H2 + Fe
D. 2K + FeCl3 → KCl + FeCl2
Lời giải:
Đáp án A
Câu 2. Khi cho K tác dụng với dung dịch muối sắt(II)clorua thu được kết tủa X. Nung kết tủa X trong không khí đến khối lượng không đổi thu được chất rắn Z. Chất rắn Z là:
A. Fe3O4 B. Fe
C. FeO D. Fe2O3
Lời giải:
Đáp án D
2K + FeCl2 + 2H2O → 2KCl + H2 + Fe(OH)2
2Fe(OH)2 + H2O + 1/2O2 → 2Fe(OH)3
2Fe(OH)3 → Fe2O3 + 3H2O
Câu 3. Cho 3,9 g K tác dụng với dung dịch FeCl2 thu được V lít khí thoát ra đktc.
Giá trị của V là:
A. 2,24 lít B. 1,12 lít
C. 1,68 lít D. 0,56 lít
Lời giải:
Đáp án B
Phương trình hóa học: 2K + FeCl2 + 2H2O → 2KCl + H2 + Fe(OH)2
nH2 = nK/2 = 0,1/2 = 0,05 mol ⇒ VH2 = 0,05.22,4 = 1,12 lít
Xem thêm các phương trình phản ứng hóa học khác:
K + AlCl3 + H2O → KCl + H2 + Al(OH)3
K + ZnCl2 + 2H2O → KCl + H2 + Zn(OH)2
K + FeCl3 + H2O → KCl + H2 + Fe(OH)3
K + Cr2(SO4)3 + H2O → K2SO4 + H2 + Cr(OH)3
K + CrCl3 + H2O → KCl + H2 + Cr(OH)3
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.





