Phản ứng K + C6H5OH → C6H5OK + H2
1. Phản ứng hóa học
2K + 2C6H5OH → 2C6H5OK + H2
2. Điều kiện phản ứng
Không cần điều kiện.
3. Cách thực hiện phản ứng
Cho kali tác dụng với phenol.
4. Hiện tượng nhận biết phản ứng
K tan dần trong và có khí thoát ra.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của K (Kali)
Trong phản ứng trên K là chất khử.
5.2. Bản chất của C6H5OH (Phenol)
– Trong phản ứng trên C6H5OH là chất oxi hoá.
– C6H5OH có tính axit yếu có phản ứng với các kim loại kiềm, dung dịch bazo.
6. Tính chất hoá học của K
Kali là kim loại kiềm có tính khử rất mạnh.
K → K+ + 1e
6.1. Tác dụng với phi kim
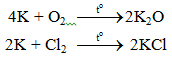
6.2. Tác dụng với axit
2K + 2HCl → 2KCl + H2.
6.3. Tác dụng với nước
K tác dụng mãnh liệt với nước và tự bùng cháy tạo thành dung dịch kiềm và giải phóng khí hidro.
2K + 2H2O → 2KOH + H2.
6.4. Tác dụng với hidro
Kali tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 – 400oC tạo thành kali hidrua.
2K (lỏng) + H2 (khí) → 2KH (rắn)
7. Tính chất vật lí của K
Kali là kim loại nhẹ thứ hai sau liti, là chất rắn rất mềm, dễ dàng cắt bằng dao và có màu trắng bạc. – Kali bị ôxi hóa rất nhanh trong không khí và phải được bảo quản trong dầu mỏ hay dầu lửa. – Có khối lượng riêng là 0,863 g/cm3; có nhiệt độ nóng chảy là 63,510C và sôi ở 7600C.
8. Tính chất hóa học của Phenol
Nhân hút e, –OH đẩy e.
8.1. Phản ứng thế nguyên tử hiđro của nhóm OH
* Tác dụng với kim loại kiềm:
C6H5OH + Na → C6H5ONa (Natri phenolat) + 1/2 H2↑
* Tác dụng với bazơ:
C6H5OH (rắn, không tan) + NaOH → C6H5ONa (tan, trong suốt) + H2O
→ Phenol có tính axit, tính axit của phenol rất yếu; dung dịch phenol không làm đổi màu quỳ tím.
Chú ý: tính axit yếu, không làm đổi màu quỳ tím, thứ tự: nấc II của H2CO3 < phenol < nấc I của H2CO3.
⇒ Có phản ứng:
C6H5ONa (dd trong suốt) + H2O + CO2 → C6H5OH (vẩn đục) + NaHCO3
C6H5OH + Na2CO3 → C6H5ONa + NaHCO3
8.2. Phản ứng thế nguyên tử hiđro của vòng benzen
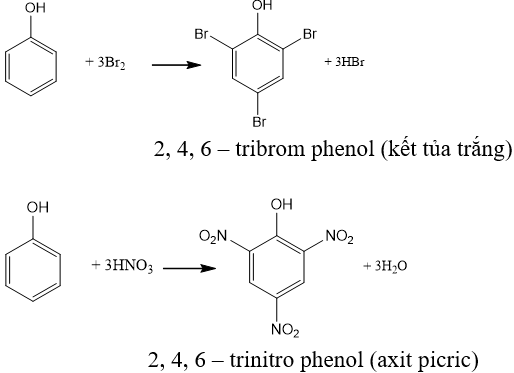
+ Phản ứng với H2:

+ Phản ứng trùng ngưng với fomandehit:
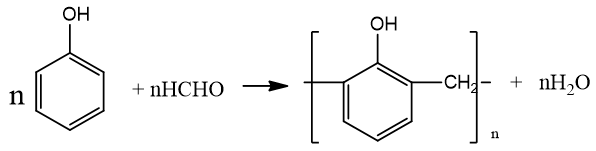
9. Câu hỏi vận dụng
Câu 1. Ở dạng lỏng, phenol và ancol benzylic đều phản ứng với
A. dung dịch NaCl.
B. dung dịch NaHCO3.
C. dung dịch NaOH.
D. kim loại K.
Lời giải:
Đáp án D
Phương trình hóa học:
2K + 2C6H5OH → 2C6H5OK + H2
2C6H5CH2OH + 2K → 2C6H5CH2OK + H2
Câu 2. Phenol phản ứng được với tất cả các chất trong dãy nào sau đây?
A. H2SO4; NaOH; NaHCO3.
B. K; Br2; CH3COOH.
C. K; NaOH; (CH3CO)2O.
D. Br2; HCl; KOH.
Lời giải:
Đáp án B
Phương trình hóa học:
2K + 2C6H5OH → 2C6H5OK + H2
2NaOH + 2C6H5OH → 2C6H5ONa + H2O
C6H5OH + (CH3CO)2O → C6H5OCOCH3 + CH3COOH
Câu 3. Cho m g K tác dụng với 9,4 g phenol phản ứng xảy ra hoàn toàn. Giá trị của m là:
A. 3,9 g B. 0,39 g
C. 1,95 g D.0,195 g
Lời giải:
Đáp án A
Phương trình hóa học: 2K + 2C6H5OH → 2C6H5OK + H2
nK = nC6H5OH = 0,1 mol
Khối lượng muối: m = 0,1.39 = 3,9 g
Xem thêm các phương trình phản ứng hóa học khác:
K2O + CO2 → K2CO3
K2O + SO2 → K2SO3
K2O + HCl → KCl + H2O
K2O + H2SO4 → K2SO4 + H2O
K2O + HNO3 → KNO3 + H2O
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.





