Phản ứng K2CO3 + Cl2 → KCl + KClO + CO2
1. Phản ứng hóa học
K2CO3 + Cl2 → KCl + KClO + CO2
2. Điều kiện phản ứng
Điều kiện thường,
3. Cách thực hiện phản ứng
Sục khí clo vào ống nghiệm chứa K2CO3.
4. Hiện tượng nhận biết phản ứng
Có khí không màu thoát ra.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của K2CO3 (Kali cacbonat)
K2CO3 là muối của axit yếu tác dụng được với Cl2.
5.2. Bản chất của Cl2 (Clo)
– Trong phản ứng trên Cl2 vừa là chất khử vừa là chất oxi hóa.
– Khi cho Cl2 vào K2CO3, clo sẽ tác dụng với nước, tạo thành axit: Cl2 + H2O ⇌ HCl + HClO. Axit sinh ra phản ứng với K2CO3 giải phóng CO2.
6. Tính chất hóa học của K2CO3
Là một muối của axit cacbonic và một muối yếu nên K2CO3 có tính chất sau:
– Tác dụng với axit mạnh hơn để tạo thành muối mới như CH3COOH, H2SO3, HNO3, HCl ….
-
- K2CO3 + 2CH3COOH → 2CH3COOK + CO2↑ + H2O
- K2CO3 + H2SO4 → K2SO4 + CO2↑ + H2O
– K2CO3 phản ứng với dung dịch kiềm để tạo muối:
-
- K2CO3 + NaOH → Na2CO3 + KOH
– K2CO3 tác dụng với dung dịch muối để tạo muối mới bền vững hơn:
-
- K2CO3 + NaCl → KCl + Na2CO3
– Do là một muối axit yếu nên K2CO3 dễ bị phân hủy ở nhiệt độ cao để giải phóng ra khí cacbonic:
-
- K2CO3 → K2O + CO2
7. Tính chất hóa học của Cl2
7.1. Tác dụng với kim loại
Đa số kim loại và có to để khơi màu phản ứng tạo muối clorua (có hoá trị cao nhất)
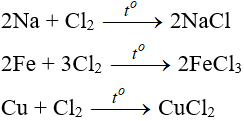
7.2. Tác dụng với phi kim
(cần có nhiệt độ hoặc có ánh sáng)
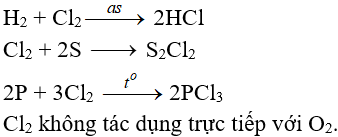
7.3. Tác dụng với nước và dung dịch kiềm
Cl2 tham gia phản ứng với vai trò vừa là chất oxi hóa, vừa là chất khử.
Tác dụng với nuớc:
Khi hoà tan vào nước, một phần Clo tác dụng (Thuận nghịch)
Cl20 + H2O → HCl + HClO (Axit hipoclorơ)
Axit hipoclorơ có tính oxy hoá mạnh, nó phá hửy các màu vì thế nước clo hay clo ẩm có tính tẩy màu do.
Tác dụng với dung dịch bazơ:
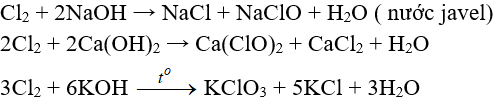
7.4. Tác dụng với muối của các halogen khác
Cl2 + 2NaBr → 2NaCl + Br2
Cl2 + 2FeCl2 → 2FeCl3
3Cl2 + 6FeSO4 → 2Fe2(SO4)3 + 2FeCl3
Cl2 + 2KI → 2KCl + I2
7.5. Tác dụng với chất khử khác
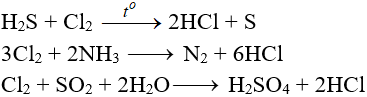
7.6. Phản ứng thế, phản ứng cộng, phản ứng phân huỷ với một số hợp chất hữu cơ
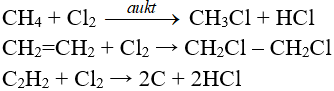
7.7. Ứng dụng của Cl2
Ứng dụng chủ yếu nhất của clo là dùng để điều chế nhựa PVC cũng như các chất dẻo hay cao su. Ngoài ra, với tính oxi hóa và tính khử, CLORAMIN còn được dùng để khử trùng nước sinh hoạt. Clo còn là một trong những thành phần để điều chế nước javen tẩy trắng quần áo, vải sợi…
8. Câu hỏi vận dụng
Câu 1. Sục khí clo vào ống nghiệm chứa K2CO3 thu được hiện tượng là
A. Có khí không màu thoát ra.
B. Có khí màu nâu đỏ thoát ra.
C. Có kết tủa vàng.
D. Không có hiện tượng gì.
Lời giải:
K2CO3 + Cl2 → KCl + KClO + CO2
CO2: khí không màu,
Đáp án A.
Câu 2. Thể tích khí CO2 ở dktc thoát ra khi cho 13,8g K2CO3 phản ứng hoàn toàn với lượng dư Cl2 là
A. 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít.
Lời giải:
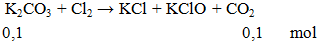
V = 0,1.22,4 = 2,24 lít.
Đáp án B.
Câu 3. Thể tích khí Cl2 đktc cần dung để phản ứng hoàn toàn với K2CO3 thu được 0,1 mol CO2 la
A. 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít.
Lời giải:
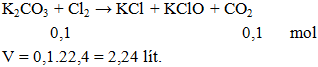
Đáp án B.
Xem thêm các phương trình hóa học khác:
K2CO3 + H2SO4 → K2SO4 + CO2 + H2O
K2CO3 + HNO3 → KNO3 + CO2 + H2O
K2CO3 + Ba(OH)2 → KOH + BaCO3
K2CO3 + Ca(OH)2 → KOH + CaCO3
K2CO3 + CaCl2 → KCl + CaCO3
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.





