Phản ứng: Al + NH3 → AlN + H2
1. Phương trình phản ứng giữa Al và NH3
2Al + 2NH3 → 2AIN + 3H2
2. Điều kiện phản ứng Al+NH3
– Nhiệt độ: 800-900 độ C
3. Cách thực hiện phản ứng Al+NH3
Cho bột nhôm nung nóng trong khoảng 800 đến 900 độ C và để bột nhôm này trên thành ống nghiệm. Sau đó, dẫn một luồng khí NH3 đi qua khối bột nhôm núng nóng trên sẽ xảy ra phản ứng giữa Al và NH3.
4. Hiện tượng sau khi phản ứng
Nhôm tác dụng với NH3 tạo thành nhôm nitrua và có khí H2 thoát ra. Trong đó, bột AlN có màu trắng vàng khí thoát ra đốt trong ống nghiệm sẽ phản ứng với oxi tạo thành nước đọng trên thành ống nghiệm.
5. Bản chất của các chất tham gia phản ứng
5.1 Bản chất của Al
Nhôm tác dụng với NH3 tạo thành nhôm nitrua và có khí H2 thoát ra.
5.2 Bản chất của NH3
Amoniac Nguyên tử hidro trong amoniac có thể bị thế bởi nguyên tử kim loại kiềm hoặc nhôm
6. Tính chất hóa học của Al
Nhôm là kim loại có tính khử mạnh: Al → Al3+ + 3e
6.1. Tác dụng với phi kim
a) Tác dụng với oxi
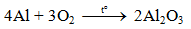
Al bền trong không khí ở nhiệt độ thường do có lớp màng oxit Al2O3 rất mỏng bảo vệ.
b) Tác dụng với phi kim khác
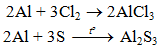
6.2. Tác dụng với axit
+ Axit không có tính oxi hóa: dung dịch axit HCl, H2SO4 loãng
2Al + 6HCl → 2AlCl3 + 3H2↑
+ Axit có tính oxi hóa mạnh: dung dịch HNO3 loãng, HNO3 đặc, nóng và H2SO4 đặc, nóng.
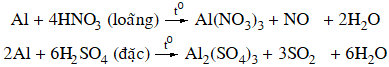
Nhôm bị thụ động hoá trong dung dịch HNO3 đặc, nguội hoặc H2SO4 đặc nguội.
6.3. Tác dụng với oxit kim loại( Phản ứng nhiệt nhôm)
Lưu ý: Nhôm chỉ khử oxit của các kim loại đứng sau nhôm
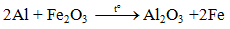
6.4. Tác dụng với nước
– Phá bỏ lớp oxit trên bề mặt Al (hoặc tạo thành hỗn hống Al-Hg thì Al sẽ phản ứng với nước ở nhiệt độ thường)
2Al + 6H2O → 2Al(OH)3↓ + 3H2↑
6.5. Tác dụng với dung dịch kiềm
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
6.6. Tác dụng với dung dịch muối
– Al đẩy được kim loại đứng sau ra khỏi dung dịch muối của chúng:
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
7. Tính chất hóa học của NH3
7.1. Tính bazơ yếu
– Tác dụng với nước:
NH3 + H2O ⇋ NH4+ + OH–
⇒ Dung dịch NH3 là một dung dịch bazơ yếu.
– Tác dụng với dung dịch muối (muối của những kim loại có hidroxit không tan):
AlCl3 + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4Cl
Al3+ + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4+
– Tác dụng với axit → muối amoni:
NH3 + HCl → NH4Cl (amoni clorua)
2NH3 + H2SO4 → (NH4)2SO4 (amoni sunfat)
7.2. Khả năng tạo phức
Dung dịch amoniac có khả năng hòa tan hiđroxit hay muối ít tan của một số kim loại, tạo thành các dung dịch phức chất.
Ví dụ:
* Với Cu(OH)2:
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2 (màu xanh thẫm)
* Với AgCl:
AgCl + 2NH3 → [Ag(NH3)2]Cl
Sự tạo thành các ion phức là do sự kết hợp các phân tử NH3 bằng các electron chưa sử dụng của nguyên tử nitơ với ion kim loại.
7.3. Tính khử
– Amoniac có tính khử: phản ứng được với oxi, clo và khử một số oxit kim loại (Nitơ có số oxi hóa từ -3 đến 0, +2).
– Tác dụng với oxi:
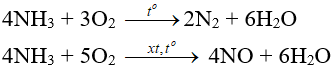
– Tác dụng với clo:
2NH3 + 3Cl2 → N2 + 6HCl
NH3 kết hợp ngay với HCl vừa sinh ra tạo “khói trắng” NH4Cl
– Tác dụng với CuO:
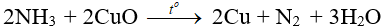
8. Ví dụ minh họa Al+NH3
Ví dụ 1: Cho dd NH3 dư vào dd AlCl3 và ZnCl2 thu được A. Nung A được chất rắn B. Cho luồng H2 đi qua B nung nóng sẽ thu được chất rắn:
A. Zn và Al
B. Zn và Al2O3
C. ZnO và Al2O3
D. Al2O3
Đáp án: D
Hướng dẫn giải
Cho NH3 dư vào thì kết tủa thu được chỉ có Al(OH)3, nung nóng X thì thu được Y sẽ là Al2O3. CO không có phản ứng với Al2O3 nên chất rắn thu được là Al2O3.
Ví dụ 2: Chỉ dùng 1 chất để phân biệt 3 kim loại sau: Al, Ba, Mg
A. Dung dịch HCl
B. Nước
C. Dung dịch NaOH
D. Dung dịch H2SO4
Đáp án: B
Hướng dẫn giải
Thấy kim loại tan dần trong nước và tạo khí là Ba:
Ba + 2H2O → Ba(OH)2 + H2↑
Cho lần lượt kim loại Al, Mg vào dung dịch Ba(OH)2 nếu kim loại tan và tạo khí là Al, còn lại là Mg
2Al + Ba(OH)2 + 6H2O → Ba[Al(OH)4]2 + 3H2↑
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.




