C2H2 (Axetilen) là gì?

1. Định nghĩa Axetilen
– Định nghĩa: Axetilen là hiđrocacbon không no nằm strong dãy đồng đẳng của ankin.Axetilen là chất khí, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí (d=26/29 ).
– Công thức phân tử: C2H2.
– Công thức cấu tạo:
![]()
– Danh pháp: Tên quốc tế: C2H2 được gọi là axetilen.
2. Tính chất vật lí của Axetilen
Axetilen là chất khí, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí (d= 26/29 ).
3. Tính chất hóa học của Axetilen
3.1. Phản ứng cộng
– Cộng brom
Trong liên kết ba của phân tử axetilen có hai liên kém bền. Vì vậy, ta axetilen sẽ làm mất màu dung dịch brom tương tự etilen.
– Dẫn axetilen qua dung dịch brom màu da cam.
+ Hiện tượng: Dung dịch brom bị mất màu.
Axetilen có phản ứng cộng với brom trong dung dịch.
![]()
+ Sản phẩm mới sinh ra có liên kết đôi trong phân tử nên có thể cộng tiếp với một phân tử brom nữa:
![]()
+ Trong điều kiện thích hợp, axetilen cũng có phản ứng cộng với hiđro và một số chất khác.
– Cộng hiđro
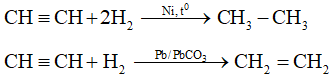
– Cộng hiđro clorua
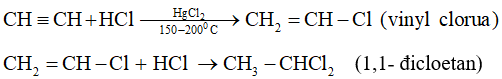
– Cộng nước (hiđrat hóa)
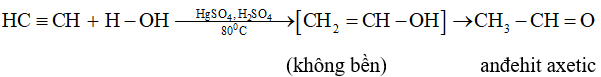
3.2. Phản ứng đime hóa và trime hóa
Hai phân tử axetilen có thể cộng hợp với nhau tạo thành vinylaxetilen
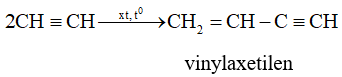
3.3. Phản ứng thế bằng ion kim loại
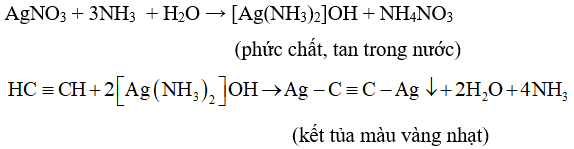
3.4. Phản ứng oxi hóa
– Axetilen là hiđrocacbon, vì vậy khi đốt, axetilen sẽ cháy tạo ra cacbon Đioxit và nước, tương tự metan và etilen.
– Axetilen cháy trong không khí với ngọn lửa sáng, tỏa nhiều nhiệt.
![]()
4. Điều chế Axetilen
– Phương pháp chính điều chế axetilen trong công nghiệp hiện nay là nhiệt phân metan ở nhiệt độ 15000 , phản ứng thu nhiệt mạnh:
Nhiệt độ sôi của axetilen là -75 nên dễ được tách ra khỏi hỗn hợp với hiđro.
– Ở những nơi dầu khí chưa phát triển, người ta điều chế axetilen theo sơ đồ sau:
![]()
– Canxi cacbua sản xuất trong công nghiệp (từ vôi sống và than đá) là chất rắn màu đen xám, trước kia được dùng tạo ra C2H2 để thắp sáng vì vậy nó được gọi là “đất đèn”.
– Ngày nay, để điều chế một lượng nhỏ axetilen trong phòng thí nghiệm hoặc trong hàn xì, người ta vẫn thường dùng đất đèn.
– Axetilen điều chế từ đất đèn thường có tạp chất (H2S, NH3, PH3,… ) có mùi khó chịu được gọi là mùi đất đèn.
![]()
5. Ứng dụng Axetilen
– Khi axetilen cháy trong oxi, nhiệt độ ngọn lửa có thể lên tới nhiệt độ 3000. Vì vậy, axetilen được dùng làm nhiên liệu trong đèn xì oxi – axetilen để hàn cắt kim loại.
– Trong công nghiệp, axetilen là nguyên liệu để sản xuất poli(vinyl clorua) (dùng để sản xuất nhựa PVC), cao su, axit axetic và nhiều hóa chất khác.
– Lưu ý, khi sử dụng axetilen phải rất cẩn trọng vì khi nồng độ axetilen trong không khí từ 2,5% trở nên có thể gây cháy nổ.
6. Bài tập về C2H2
Ví dụ 1. Cho 0,56 lít (đktc) hỗn hợp khí metan và axetilen tác dụng với dung dịch brom dư, lượng brom đã tham gia phản ứng là 5,6 gam. Thành phần phần trăm về thể tích của axetilen trong hỗn hợp ban đầu lần lượt là
A. 20%.
B. 70%.
C . 40%.
D. 60%.
Hướng dẫn giải:
Đáp án B
Ta có:
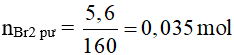
Cho hỗn hợp khí qua dung dịch brom dư chỉ có axetilen phản ứng
HC≡CH + 2Br2 → Br2CH–CHBr2
0,0175 ← 0,035 mol
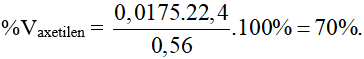
Ví dụ 2: Nêu phương pháp làm sạch khí O2 bị lẫn các khí C2H4 và C2H2. Viết các phương trình phản ứng hoá học xảy ra (nếu có).
Hướng dẫn giải:
Cho hỗn hợp khí đi qua bình đựng lượng dư brom, C2H4 và C2H2 phản ứng với Br2 bị giữ lại trong bình; O2 không phản ứng thoát ra thu được O2 tinh khiết.
C2H4 + Br2 → C2H4Br2
C2H2 + 2Br2 → C2H2Br4
Ví dụ 3: Đốt cháy hoàn toàn 11,2 lít hỗn hợp khí gồm C2H4 ; C2H2 thu được khí CO2 và 12,6 gam nước. Tính phần trăm thể tích của mỗi khí trong hỗn hợp (thể tích các khí đều đo ở đktc)
Hướng dẫn giải:
Gọi số mol của C2H4 và C2H2 lần lượt là x mol và y mol.
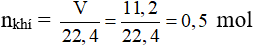
→ x + y = 0,5 (1)
PTHH:
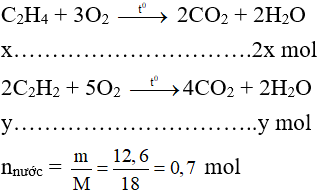
Theo các PTHH có: nnước = 2x + y = 0,7 (2)
Từ (1) và (2) có x = 0,2 mol và y = 0,3 mol.
Do các khí ở cùng điều kiện nên tỉ lệ về thể tích cũng chính là tỉ lệ về số mol
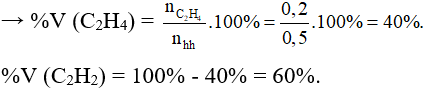
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.





