Phản ứng KOH + KHS → K2S + H2O
1. Phản ứng hóa học
KOH + KHS → K2S + H2O
2. Điều kiện phản ứng
Điều kiện thường.
3. Cách thực hiện phản ứng
Nhỏ từ từ KOH vào ống nghiệm có chứa KHS và vài giọt chỉ thị.
4. Hiện tượng nhận biết phản ứng
Quan sát sự chuyển màu của chỉ thị.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của KOH (Kali hidroxit)
KOH là một bazo mạnh có thể phản ứng với muối hidro sunfua để thu được muối sunfua.
5.2. Bản chất của KHS (Kali hidrosunfua)
KHS là muối hido sunfua tác dụng được với KOH.
6. Tính chất hoá học của KOH
KOH là một bazo mạnh có khả năng làm thay đổi màu sắc các chất chỉ thị như khiến quỳ tím chuyển sang màu xanh, còn dung dịch phenolphtalein không màu thành màu hồng.
6.1. Tác dụng với oxit axit
Ở điều kiện nhiệt độ phòng, KOH tác dụng với SO2, CO2,…
KOH + SO2 → K2SO3 + H2O
KOH + SO2 → KHSO3
6.2. Tác dụng với axit
-
Tác dụng với axit tạo thành muối và nước
KOH(dd) + HCl(dd) → KCl(dd) + H2O
-
Tác dụng với các axit hữu cơ để tạo thành muối và thủy phân este, peptit
RCOOR1 + KOH → RCOOK + R1OH
6.3. Tác dụng với kim loại
KOH tác dụng với kim loại mạnh tạo thành bazo mới và kim loại mới.
KOH + Na → NaOH + K
6.4. Tác dụng với muối
KOH tác dụng với muối để tạo thành muối mới và axit mới
2KOH + CuCl2 → 2KCl + Cu(OH)2↓
6.5. KOH điện li mạnh
KOH là một bazo mạnh, trong nước phân ly hoàn toàn thành ion K+ và OH-
6.6. KOH phản ứng với một số oxit kim loại mà oxit, hidroxit của chúng lưỡng tính
KOH phản ứng được với một số oxit kim loại mà oxit, hidroxit của chúng lưỡng tính như nhôm, kẽm,…
2KOH + 2Al + 2H2O → 2KAlO2 + 3H2↑
2KOH + Zn → K2ZnO2 + H2↑
6.7. Phản ứng với một số hợp chất lưỡng tính
KOH + Al(OH)3 → KAlO2 + 2H2O
2KOH + Al2O3 → 2KAlO2 + H2O
7. Tính chất vật lý của KOH
– Khối lượng riêng: 2.044 g/cm3
– Độ pH: 13
– Nhiệt độ sôi: 1.327oC (1.6000 K; 2.421 oF)
– Nhiệt độ nóng chảy: 406 oC (679 K; 763 oF)
– Độ hòa tan trong nước:7 g/ml (0 oC); 121 g/ml (25 oC); 178 g/ml (100 oC)
– Khả năng hòa tan chất khác: có thể được hòa tan trong alcohol, glycerol và không tan được trong ether.
8. Câu hỏi vận dụng
Câu 1. KOH không phản ứng với dung dịch nào sau đây?
A. KHS. B. NaHS C. K2S. D. H2S.
Lời giải:
K2S không phản ứng với KOH.
Đáp án C.
Câu 2. Dẫn từ từ đến dư H2S vào dung dịch KOH thu được dung dịch X. Muối tan có trong dung dịch X là
A. K2S. B. K2S và KHS. C. KHS. D. K2S và KOH.
Lời giải:
Do H2S dư nên có phản ứng
KOH + H2S → KHS + H2O
Muối tan có trong dung dịch X là KHS.
Đáp án C.
Câu 3. Cho 0,56g KOH hòa tan vào nước được dung dịch X. Lượng dung dịch X trên phản ứng vừa đủ với dung dịch KHS. Khối lượng muối có trong dung dịch thu được sau phản ứng là
A. 1 gam. B, 0,1 gam. C. 0,5 gam. D. 1,1 gam.
Lời giải:
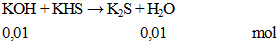
khối lượng muối = 0,01. 110=1,1 gam.
Đáp án D.
Xem thêm các phương trình hóa học khác:
KOH + NaHS → K2S + Na2S + H2O
KOH + NaHSO3 → K2SO3 + Na2SO3 + H2O
KOH + NaHCO3 → K2CO3 + Na2CO3 + H2O
K2CO3 + HBr → KBr + CO2 + H2O
K2CO3 + H2SO4 → K2SO4 + CO2 + H2O
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.




