Phản ứng: CuO + H2 → Cu + H2O
1. Phương trình phản ứng giữa CuO và H2
CuO + H2 → Cu + H2O
2. Điều kiện phản ứng
– Nhiệt độ cao.
3. Cách thực hiện phản ứng
– Cho dòng khí H2 đi qua bột CuO màu đen.
4. Hiện tượng nhận biết phản ứng
– Bột CuO màu đen chuyển dần sang màu đỏ gạch là Cu.
5. Bạn có biết
Tương tự các oxit bazơ đứng sau oxit nhôm trong dãy hoạt động hóa học (như FeO, PbO….) bị khử bởi H2 tạo thành kim loại và khí H2O.
6. Bản chất của các chất tham gia phản ứng
6.1 Bản chất của CuO
– Trong phản ứng trên CuO là chất oxi hoá.
– CuO là oxit bazo dễ bị khử về Cu khi tác dụng với các chất khử mạnh như hidro, CO, …
6.2 Bản chất của H2
Trong phản ứng trên H2 là chất khử.
7. Tính chất hóa học của CuO
– Có đầy đủ tính chất hóa học của một oxit bazơ.
– Dễ bị khử về kim loại đồng.
7.1 Tác dụng với axit
CuO + 2HCl → CuCl2 + H2O
CuO + 2HNO3 → Cu(NO3)2 + H2O
7.2 Tác dụng với oxit axit
3CuO + P2O5 → Cu3(PO4)2
7.3 Tác dụng với các chất khử mạnh: H2, C, CO…
H2 + CuO 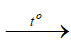 H2O + Cu
H2O + Cu
CO + CuO 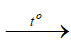 CO2 + Cu
CO2 + Cu
8. Tính chất vật lí và nhận biết
– Tính chất vật lí: Là chất rắn, có màu đen, không tan trong nước, nóng chảy ở 1148độC.
– Nhận biết: Dẫn khí H2 dư qua bột oxit đồng có màu đen, đun nóng, sau một thời gian thấy xuất hiện chất rắn màu đỏ (Cu).
H2 + CuO 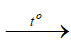 H2O + Cu
H2O + Cu
9. Tính chất hóa học của H2
9.1 Tác dụng với oxi
Nếu đốt cháy hidro trong oxi: hidro cháy mạnh, trên thành lọ xuất hiện những giọt nước nhỏ
PTHH: 2H2 + O2 → 2H2O
Hỗn hợp sẽ gây nổ nếu trộn hidro và oxi theo tỉ lệ thể tích 2:1
9.2 Tác dụng với một số oxit kim loại
– Hiđro có tính khử, khử một số oxit kim loại ở nhiệt độ cao
H2 + CuO →to Cu + H2O
màu đen màu đỏ
3H2 + Fe2O3 →to 2Fe + 3H2O
– H2 không tác dụng với các oxit: Na2O, K2O, BaO, CaO, MgO, Al2O3
10. Ví dụ minh họa
Ví dụ 1: Cho H2 dư qua 8,14 gam hỗn hợp A gồm CuO, Al2O3 và FexOy nung nóng. Sau khi phản ứng xong, thu được 1,44g H2O và a gam chất rắn. Giá trị của a là:
A. 6,70g. B. 6,86g.
C. 6,78g. D. 6,80g.
Đáp án B
Hướng dẫn giải:
nH2O = 0,08 mol
Bảo toàn nguyên tố O ⇒ nO = 0,08 mol
⇒ mchất rắn = mhỗn hợp oxit – mO = 8,14 – 16. 0,08 = 6,86g
Ví dụ 2: Khử hoàn toàn 18,0 gam một oxit kim loại M cần 5,04 lít khí H2 (đktc). Công thức của oxit là
A. Fe2O3. B. FeO.
C. ZnO. D. CuO.
Đáp án D
Hướng dẫn giải:
nH2 = 0,225mol
M2On + nH2 → M + nH2O
0,225/n ← 0,225
⇒ (0,225/n).(2M + 16n) = 18 ⇒ M = 32n ⇒ n = 2, M = 64
⇒ Công thức oxit là CuO
Ví dụ 3: Cho luồng khí H2 dư qua hỗn hợp các oxit CuO, Fe2O3, ZnO, MgO nung nóng ở nhiệt độ cao. Sau phản ứng, hỗn hợp chất rắn còn lại là :
A. Cu, Fe, ZnO, MgO.
B. Cu, Fe, Zn, Mg.
C. Cu, Fe, Zn, MgO.
D. Cu, FeO, ZnO, MgO.
Đáp án A
Hướng dẫn giải:
Các oxit kim loại đứng trước oxit nhôm là ZnO và MgO không bị khử bớt H2 còn oxit kim loại CuO và Fe2O3 đứng sau oxit nhôm bị khử bởi H2 tạo Cu và Fe.
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.




