Phản ứng K2O + HNO3 → KNO3 + H2O
1. Phản ứng hóa học
K2O + 2HNO3 → 2KNO3 + H2O
2. Điều kiện phản ứng
Phản ứng xảy ra ở điều kiện thường.
3. Cách thực hiện phản ứng
Cho K2O phản ứng với dung dịch axit HNO3.
4. Hiện tượng nhận biết phản ứng
K2O ( màu vàng nhạt) tan dần, sau phản ứng thu được dung dịch không màu.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của K2O (Kali oxit)
K2O là oxit bazo phản ứng được với các axit như HCl, H2SO4, HNO3, … thu được muối và nước.
5.2. Bản chất của HNO3 (Axit nitric)
HNO3 là một axit khan, monoaxit mạnh tác dụng được với các bazo, oxit bazo, muối cacbonat tạo thành các muối nitrat.
6. Tính chất hoá học của K2O
K2O là oxit bazo do đó mang đầy đủ tính chất hóa học của một oxit bazơ.
6.1. K2O tác dụng với nước
K2O tác dụng với nước tạo ra dung dịch kiềm KOH.
K2O + H2O → KOH
6.2. K2O tác dụng với oxit axit tạo thành muối
K2O + CO2→ K2CO3
6.3. K2O tác dụng với dung dịch axit
K2O + axit → muối + H2O
K2O + HCl → KCl + H2O
7. Tính chất vật lý của K2O
K2O là một chất bột màu trắng, không mùi, và có nhiệt độ nóng chảy khoảng 891°C
8. Tính chất hóa học của HNO3
– Axit nitric là một dung dịch nitrat hydro có công thức hóa học HNO3 . Đây là một axit khan, là một monoaxit mạnh, có tính oxy hóa mạnh có thể nitrat hóa nhiều hợp chất vô cơ, có hằng số cân bằng axit (pKa) = −2.
– Axit nitric là một monoproton chỉ có một sự phân ly nên trong dung dịch, nó bị điện ly hoàn toàn thành các ion nitrat NO3− và một proton hydrat, hay còn gọi là ion hiđroni.
H3O+ HNO3 + H2O → H3O+ + NO3-
– Axit nitric có tính chất của một axit bình thường nên nó làm quỳ tím chuyển sang màu đỏ.
– Tác dụng với bazo, oxit bazo, muối cacbonat tạo thành các muối nitrat
2HNO3 + CuO → Cu(NO3)2 + H2O
2HNO3 + Mg(OH)2 → Mg(NO3)2 + 2H2O
2HNO3 + CaCO3 → Ca(NO3)2 + H2O + CO2
– Axit nitric tác dụng với kim loại: Tác dụng với hầu hết các kim loại trừ Au và Pt tạo thành muối nitrat và nước .
Kim loại + HNO3 đặc → muối nitrat + NO + H2O ( to)
Kim loại + HNO3 loãng → muối nitrat + NO + H2O
Kim loại + HNO3 loãng lạnh → muối nitrat + H2
Mg(rắn) + 2HNO3 loãng lạnh → Mg(NO3)2 + H2 (khí)
– Nhôm, sắt, crom thụ động với axit nitric đặc nguội do lớp oxit kim loại được tạo ra bảo vệ chúng không bị oxy hóa tiếp.
– Tác dụng với phi kim (các nguyên tố á kim, ngoại trừ silic và halogen) tạo thành nito dioxit nếu là axit nitric đặc và oxit nito với axit loãng và nước, oxit của phi kim.
C + 4HNO3 đặc → 4NO2 + 2H2O + CO2
P + 5HNO3 đặc → 5NO2 + H2O + H3PO4
3C + 4HNO3 loãng → 3CO2 + 4NO + 2H2O
– Tác dụng với oxit bazo, bazo, muối mà kim loại trong hợp chất này chưa lên hóa trị cao nhất:
FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O
FeCO3 + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O + CO2
– Tác dụng với hợp chất:
3H2S + 2HNO3 (>5%) → 3Skết tủa + 2NO + 4H2O
PbS + 8HNO3 đặc → PbSO4 kết tủa + 8NO2 + 4H2O
Ag3PO4 tan trong HNO3, HgS không tác dụng với HNO3.
– Tác dụng với nhiều hợp chất hữu cơ: Axit nitric có khả năng phá hủy nhiều hợp chất hữu cơ, nên sẽ rất nguy hiểm nếu để axit này tiếp xúc với cơ thể người
9. Câu hỏi vận dụng
Câu 1. Cho m gam K2O phản ứng vừa đủ với 100ml dung dịch HNO3 1M. Giá trị của m là
A. 9,4. B. 4,7. C. 4,9. D. 7,4.
Lời giải:
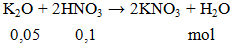
m = 0.05.94 = 4,7 gam.
Đáp án B.
Câu 2. Chất nào sau đây không tác dụng với HNO3?
A. KOH. B. K2O. C. K. D. KNO3.
Lời giải:
KNO3 không tác dụng với HNO3.
Đáp án D.
Câu 3. Cho 9,4 gam K2O tác dụng với một lượng vừa đủ dung dịch HNO3, thu được dung dịch X. Khối lượng chất tan có trong dung dịch X là
A. 10,1 gam. B. 20,2 gam. C. 10 gam. D. 19,2 gam.
Lời giải:
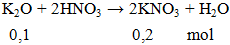
m = 0.2.101= 20,2 gam.
Đáp án B.
Xem thêm các phương trình hóa học khác:
K2O + CH3COOH → CH3COOK + H2O
K2O + HBr → KBr + H2O
K2O + HI → KI + H2O
KOH + CO2 → KHCO3
KOH + SO2 → KHSO3
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.




