Phản ứng: KNO3 → KNO2 + O2

1. Phương trình nhiệt phân KNO3
2KNO3 –to→ 2KNO2 + O2
2. Điều kiện phản ứng
– Phản ứng xảy ra khi nung nóng.
3. Cách thực hiện phản ứng
– Nhiệt phân KNO3.
4. Hiện tượng nhận biết phản ứng
– Có khí thoát ra, khối lượng chất rắn sau phản ứng giảm so với trước phản ứng.
5. Tính chất hóa học của KNO3
– KNO3 thể hiện tính oxi hóa rất cao.
– Nó bị phân hủy ở nhiệt độ cao khoảng 700 độ C để tạo ra kali nitrit và giải phóng khí oxi theo phương trình dưới đây.
2KNO3 → 2KNO2 + O2
6. Ứng dụng của KNO3
KNO3 trong phân bón có vai trò:
– Cung cấp nguồn kali, nitơ cần thiết đối với sự phát triển của cây và hoạt động bình thường của tế bào biểu mô.
– Cation K+ giúp điều hòa và tham gia vào sự đóng mở của lỗ khí khổng đối với quá trình thoát hơi nước của cây.
– Giúp cho cây trồng khỏe mạnh, tăng năng suất cây trồng.
– Giảm độ mặn của đất, giúp tiết kiệm nước khi trồng.
– Đóng vai trò quan trọng trong dinh dưỡng thủy canh bởi vì KNO3 tác động đến sự phát triển của cây trồng. Nếu không cung cấp đủ kali và nitrat cho cây, sẽ thấy cháy mép lá, đốm đen và vàng lá.
– KNO3 giúp chống lại vi khuẩn, nấm, côn trùng và virus gây bệnh. Đồng thời nó còn làm giảm đáng kể sự hấp thụ Cl- của cây trồng và chống lại các tác nhân gây hại của natri.
7. Bạn có biết
– Tương tự như KNO3, các muối nitrat của kim loại hoạt động mạnh bị phân hủy tạo ra muối nitrit và oxi.
8. Ví dụ minh họa
Ví dụ 1:
Nhiệt phân muối KNO3 thu được sản phẩm là
A. KNO2, O2. B. K2O, O2. C. K2O, NO2, O2. D. K, NO2, O2.
Hướng dẫn giải
2KNO3 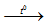 2KNO2 + O2
2KNO2 + O2
Đáp án A.
Ví dụ 2:
Nhiệt phân muối nitrat nào sau không thu được muối nitrit?
A. KNO3. B. NaNO3. C. LiNO3. D. Mg(NO3)2.
Hướng dẫn giải
2Mg(NO3)2 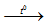 2MgO + 4NO2 + O2
2MgO + 4NO2 + O2
Đáp án D.
Ví dụ 3:
Thể tích khí ở đktc thoát ra khi nhiệt phân hoàn toàn 10,1g KNO3 là
A. 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít.
Hướng dẫn giải
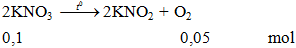
V = 0.05.22,4= 1,12 lít.
Đáp án A.
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.




