Phản ứng NH3 + H3PO4 → (NH4)3PO4
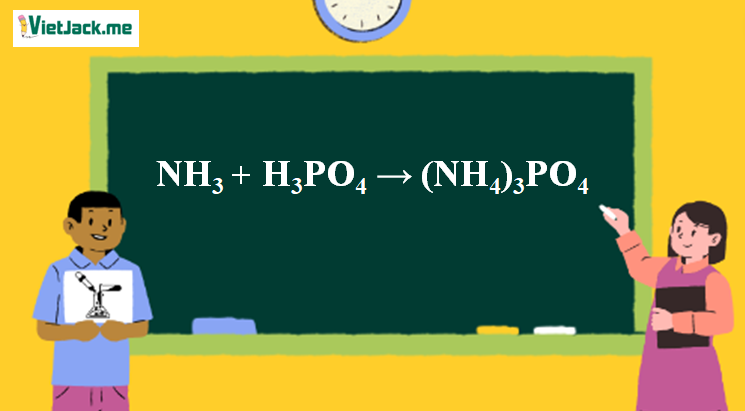
1. Phương trình phản ứng NH3 tác dụng H3PO4
3NH3 + H3PO4 → (NH4)3PO4
2. Bản chất của phương trình NH3 tác dụng với H3PO4
(1): NH3 + H3PO4 → NH4H2PO4
(2): 2NH3 + H3PO4 → (NH4)2HPO4
(3): 3NH3 + H3PO4 → (NH4)3PO4
gọi n= số mol của NH3/H3PO4
+ Nếu n = 1: chỉ có phản ưng (1)
sản phẩm suy nhất là: NH4H2PO4
+ Nếu 1 < n < 2: xảy ra phản ứng (1) và (2)
tạo hai muối NH4H2PO4và (NH4)2HPO4.
+ Nếu n = 2: xảy ra phản ứng (2)
sản phẩm duy nhất là: (NH4)2HPO4
+ Nếu 2 < n < 3: xảy ra phản ứng (2) và (3)
tạo hai muối (NH4)2HPO4và (NH4)3PO4
+ Nếu n = 3: xảy ra phản ứng (3)
sản phẩm suy nhất là: (NH4)3PO4
3. Tính chất hoá học của NH3
3.1. Amoniac có tính bazơ yếu
Amoniac do tính bazơ nên dung dịch amoniac làm cho quỳ tím hóa xanh còn dung dịch phenolphlatein từ màu chuyển thành hồng.
Do đó để phát hiện amoniac, người ta dùng quỳ tím ẩm để nhận biết.
Nguyên nhân: do cặp e chưa tham gia liên kết ở nguyên tử N
Ba(OH)2 > NaOH > NH3 > Mg(OH)2 > Al(OH)3
a) Amoniac phản ứng với nước
NH3 + H2O ⇔ NH4+ + OH–
b) Amoniac phản ứng với Axit → Muối Amoni
Thí dụ:
NH3 (khí) + HCl (khí) → NH4Cl (khói trắng)
NH3 + H2SO4 → NH4HSO4
2NH3 + H2SO4 → (NH4)2SO4
c) Amoniac tác dụng với dung dịch muối của các kim loại mà hidroxit không tan → bazơ và muối
NH3 + Muối (dung dịch) → Bazơ + Muối mới
Thí dụ
2NH3+ MgCl2 + 2H2O → Mg(OH)2 + 2NH4Cl
3NH3 + AlCl3+ 3H2O →Al(OH)3↓ + 3NH4Cl
* Chú ý: Với muối của Cu2+, Ag+ và Zn2+ có kết tủa sau đó kết tủa tan do tạo phức chất tan
Cu(NH3)4(OH)2; Ag(NH3)2OH; Zn(NH3)4(OH)2.
Thí dụ:
ZnSO4+ 2NH3+ 2H2O → Zn(OH)2↓ + (NH4)2SO4
Zn(OH)2 + 4NH3 → [Zn(NH3)3](OH)2
3.2. Amoniac có tính khử mạnh
Nguyên nhân: do N trong NH3 có mức oxi hóa thấp nhất -3
a) Amoniac tác dụng với O2
4NH3 + 3O2 2N2↑ + 6H2O
4NH3 + 5O2 4NO↑ + 6H2O
b) Amoniac tác dụng với Cl2
2NH3 + 3Cl2 N2↑ + 6HCl
8NH3 + 3Cl2 → N2↑ + 6NH4Cl
c) Amoniac tác dụng với oxit của kim loại
Thí dụ:
3CuO + 2NH3 Cu + 3H2O + N2↑
3.3. Khả năng tạo phức
Dung dịch amoniac có khả năng hòa tan hiđroxit hay muối ít tan của một số kim loại, tạo thành các dung dịch phức chất.
Ví dụ:
* Với Cu(OH)2:
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2 (màu xanh thẫm)
* Với AgCl:
AgCl + 2NH3 → [Ag(NH3)2]Cl
Sự tạo thành các ion phức là do sự kết hợp các phân tử NH3 bằng các electron chưa sử dụng của nguyên tử nitơ với ion kim loại.
4. Tính chất hóa học của H3PO4
4.1. Tính oxi hóa – khử
Axít photphoric khó bị khử (do P ở mức oxi hóa +5 bền hơn so với N trong axit nitric), không có tính oxi hóa.
4.2. Tính axit
Axít photphoric là axit có 3 lần axit, có độ mạnh trung bình. Trong dung dịch nó phân li ra 3 nấc:
H3PO4 ⇋ H+ + H2PO4– ⇒ k1 = 7, 6.10-3
H2PO4– ⇋ H+ + HPO42- ⇒ k2 = 6,2.10-8
HPO42- ⇋ H+ + PO43- ⇒ k3 = 4,4.10-13
⇒ nấc 1 > nấc 2 > nấc 3.
⇒ Dung dịch axít photphoric có những tính chất chung của axit như làm quì tím hóa đỏ, tác dụng với oxit bazơ, bazơ, muối, kim loại.
⇒ Khi tác dụng với oxit bazơ, bazơ tùy theo lượng chất tác dụng mà axít photphoric tạo ra muối trung hòa, muối axit hoặc hỗn hợp muối:
H3PO4 + NaOH → NaH2PO4 + H2O
H3PO4 + 2NaOH → Na2HPO4 + 2H2O
H3PO4 + 3NaOH → Na3PO4 + 3H2O
5. Điều chế H3PO4
Trong phòng thí nghiệm: để điều chế ra axit photphoric trong phòng thí nghiệm người ta cho HNO3 đặc tác dụng với photpho (P) ở nhiệt độ cao, phản ứng xảy ra sẽ tạo ra H3PO4.
Phương trình phản ứng: P + 5HNO3 -> H3PO4 + 5NO2 + H2O
Trong công nghiệp: Để sản xuất ra H3PO4 người ta sử dụng chủ yếu 2 phương pháp là: Phương pháp khô và phương pháp ướt.
Phương pháp khô sử dụng nhiệt để đốt nên có thể gọi là quá trình nhiệt:
Người ta điều chế H3PO4 bằng cách đốt photpho (P) nguyên chất để tạo ra photpho pentaoxit (P2O5). Tiếp đến, hòa trong axit photphoric loãng. Sau đó, trải qua quá trình đốt nóng trong lò điện, tạp chất được loại bỏ, chúng t thu được H3PO4 nguyên chất.
Phản ứng hóa học: P → P2O5 → H3PO4
4P + 5O2 → 2P2O5
P2O5 + 3H2O → 2H3PO4
Phương pháp ướt hay còn gọi là phương pháp trích ly:
Để điều chế axit photphoric bằng phương pháp ướt người ta sử dụng Axit sunfuric (H2SO4) để phân hủy khoáng calcium phosphate-tạp chất thường tìm thấy trong tự nhiên:
Phản ứng hóa học: Ca3(PO4)2 + 3H2SO4 đặc → 3CaSO4 + 2H3PO4
6. Bài tập vận dụng liên quan
Câu 1. Dung dịch nào sau đây không làm đổi màu quì tím?
A. NaOH
B. HCl
C. KNO3
D. NH3
Lời giải:
Đáp án C
Câu 2. Trong phòng thí nghiệm ,để điều chế một lượng nhỏ khí X tinh khiết, người ta đun nóng dung dịch NH4NO3 bão hoà. Khí X là:
A. NO
B. N2O
C. N2
D. NO2
Lời giải:
Đáp án B
Câu 3. Cho 20 gam dung dịch H3PO437,11% tác dụng vừa đủ với NH3 thì thu được 10g muối photphat amoni A. Công thức của muối A là:
A. (NH4)2HPO4
B. NH4H2PO4
C. (NH4)3PO4
D. Không xác định
Lời giải:
Đáp án A
Ta có nH3PO4= 0,07573 mol
Đặt công thức của muối amoni là (NH4)nH3-nPO4
H3PO4+ nNH3 →(NH4)nH3-nPO4
Ta có nmuối= nH3PO4= 0,07573 mol→ Mmuối A= 10/ 0,07573= 132 g/mol
→ 18n + 3-n+ 95= 132 → n= 2 → Công thức của muối A là (NH4)2HPO4
Câu 4. Có các muối sau: NH4Cl, NaCl, MgSO4 đựng trong các lọ không nhãn, có thể dùng dung dịch nào sau đây để nhận biết chúng?
A. AgNO3
B. HCl
C. H2SO4
D. NaOH
Lời giải:
Đáp án D
Dùng NaOH
+ kết tủa trắng keo là MgSO4
+ kết tủa trắng xanh là FeSO4
+ kết tủa dỏ nâu là FeCl3
+ có khí mùi khai thoát ra là NH4Cl
+ không có hiện tượng là NaCl và NaOH.
Cho dung dịch FeCl3 vào 2 dung dịch còn lại
+ xuất hiện kết tủa nâu đỏ là NaOH
+ không có hiện tượng là NaCl
Câu 5. Khi nung chất rắn X ở nhiệt độ cao, người ta thu được một oxit của nitơ và hơi nước. Cho X vào dung dịch NaOH thấy có khí mùi khai thoát ra. X là
A. (NH4)2SO4.
B. NH4NO2.
C. NH4HCO3.
D. NH4NO3.
Lời giải:
Đáp án D
Khí mùi khai thoát ra là NH3
Vì nhiệt phân X thu được oxit của nitơ và nước => trong phân tử X chỉ gồm N, H và O
=> X là NH4NO3
Loại B vì NH4NO2 → N2 + 2H2O
Câu 6. Khi cho dung dịch Ba(OH)2 vào dung dịch (NH4)2SO4 và đun nóng có hiện tượng:
A. chỉ có kết tủa trắng.
B. có kết tủa trắng và khí mùi khai bay lên.
C. chỉ có khí mùi khai bay lên.
D. có kết tủa trắng sau đó kết tủa tan.
Lời giải:
Đáp án B
Phương trình phản ứng minh họa:
Ba(OH)2 + (NH4)2SO4→ BaSO4↓ + 2NH3↑ + 2H2O
Khi cho dung dịch Ba(OH)2 vào dung dịch (NH4)2SO4 và đun nóng có hiện tượng có kết tủa trắng và khí mùi khai bay lên.
Câu 7. Sử dụng dung dịch Ba(OH)2 có thể phân biệt dãy dung dịch muối nào sau đây:
A. MgCl2, NH4Cl, Na2SO4, NaNO3.
B. AlCl3, ZnCl2, NH4Cl, KCl.
C. NH4Cl, (NH4)2SO4, K2SO4, NaNO3.
D. NH4NO3, NH4Cl, K2SO4, KCl.
Lời giải:
Đáp án C
Xem thêm các phương trình hóa học khác:
NH3 + HNO3 → NH4NO3
NH3 + Cl2 → N2 + NH4Cl
NH3 + O2 → NO + H2O
NH3 + HCl → NH4Cl
NH3 + H2O → NH4OH
NH3 + AlCl3 + H2O → Al(OH)3 + NH4Cl
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.




