Phản ứng NH4Cl + AgNO3 → NH4NO3 + AgCl
1. Phương trình phản ứng NH4Cl ra NH4NO3
NH4Cl + AgNO3 → NH4NO3 + AgCl↓trắng
2. Phương trình ion thu gọn NH4Cl + AgNO3
Nhỏ dung dịch NH4Cl vào ống nghiệm đựng dung dịch AgNO3 sẽ tạo thành phương trình phản ứng.
NH4Cl + AgNO3 → NH4NO3 + AgCl ↓
NH4Cl và AgNO3 là các chất dễ tan và phân li mạnh
NH4Cl → NH4+ + Cl–
AgNO3 → Ag+ + NO3–
Trong dung dịch các ion Ag+ sẽ kết hợp với ion NO3– tạo thành chất kết tủa màu trắng AgCl
Phương trình ion thu gọn
Cl− + Ag+ → AgCl
3. Điều kiện phản ứng NH4Cl tác dụng với AgNO3
Nhiệt độ thường
4. Hiện tượng cho dung dịch AgNO3 phản ứng NH4Cl
Khi cho dung dịch AgNO3 tác dụng với NH4Cl, sau phản ứng xuất hiện kết tủa trắng bạc clorua (AgCl). Đây cũng chính là phương trình dùng để nhận biết muối amoni clorua.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của NH4Cl (Amoni clorua)
NH4Cl là chất tan tốt trong nước và phân li rất mạnh.
5.2. Bản chất của AgNO3 (Bạc nitrat)
AgNO3 là chất dễ hoà tan trong nước và phân li mạnh. Ag+ sẽ kết hợp với ion NO3– tạo thành kết tủa màu trắng AgCl. (Chú ý: Phản ứng nhận biết muối amoni clorua)
6. Tính chất hoá học của muối amoni
6.1.Phản ứng thuỷ phân
Tạo môi trường có tính axit làm quỳ tím hoá đỏ.
NH4+ + HOH → NH3 + H3O+ (Tính axit)
6.2. Tác dụng với dung dịch kiềm
(nhận biết ion amoni, điều chế amoniac trong phòng thí nghiệm)
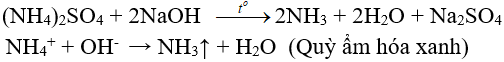
6.3. Phản ứng nhiệt phân
– Muối amoni chứa gốc của axit không có tính oxi hóa khi nung nóng bị phân hủy thành NH3.
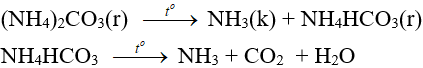
NH4HCO3 (bột nở) được dùng làm xốp bánh.
– Muối amoni chứa gốc của axit có tính oxi hóa khi bị nhiệt phân cho ra N2, N2O.
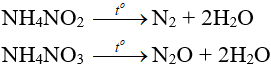
– Nhiệt độ lên tới 500oC, ta có phản ứng:
2NH4NO3 → 2N2 + O2 + 4H2O
7. Mở rộng kiến thức về AgNO3
7.1. Tính chất vật lí & nhận biết
– Tính chất vật lí: Là chất rắn, có màu trắng, tan tốt trong nước, có nhiệt độ nóng chảy là 212oC.
– Nhận biết: Sử dụng muối NaCl, thu được kết tủa trắng
AgNO3 + NaCl →AgCl↓+ NaNO3
7.2. Tính chất hóa học
– Mang tính chất hóa học của muối
Tác dụng với muối
AgNO3 + NaCl →AgCl↓+ NaNO3
2AgNO3 + BaCl2 →2AgCl↓+ Ba(NO3)2
Tác dụng với kim loại:
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Tác dụng với axit:
AgNO3 + HI → AgI ↓ + HNO3
Oxi hóa được muối sắt (II)
Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
7.3. Điều chế
Bạc nitrat điều chế bằng cách hòa tan kim loại bạc trong dung dịch axit nitric.
3Ag + 4 HNO3(loãng) → 3AgNO3 + 2H2O + NO
3Ag + 6 HNO3(đặc, nóng) → 3AgNO3 + 3 H2O + 3NO2
7.4. Ứng dụng
AgNO3 được sử dụng để sản xuất muối bạc khác. AgNO3 được sử dụng để tạo ra chất kết dính dẫn điện, máy lọc khí mới, sàng phân tử A8x , quần áo cân bằng áp suất mạ bạc và găng tay để làm việc trực tiếp. AgNO3 được sử dụng để làm vật liệu nhạy sáng cho phim, phim x-quang và phim ảnh.
8. Bài tập vận dụng liên quan
Câu 1. Dung dịch nào sau đây phản ứng với NH4Cl sinh ra NH3?
A. Ca(OH)2.
B. NaNO3.
C. HNO3.
D. NaCl.
Lời giải:
Câu 2. Cặp dung dịch nào sau đây phản ứng với nhau tạo ra chất khí?
A. NH4Cl và AgNO3.
B. NaOH và H2SO4.
C. Ca(OH)2 và NH4Cl.
D. K2CO3 và NaOH.
Lời giải:
NH4Cl + AgNO3 → NH4NO3 + AgCl↓
2NaOH + H2SO4 → Na2SO4 + 2H2O
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 ↑ + 2H2O
K2CO3 + 2NaOH → Na2CO3 + 2KOH
Câu 3. Thuốc thử dùng để nhận biết các dung dịch NH4Cl, (NH4)2SO4, K2SO4 và KCl là:
A. KOH
B. Quì tím
C. Ba(OH)2
D. CaCl2
Lời giải:
Để nhận biết 4 chất trên ta có thể dùng Ba(OH)2
Trích mẫu và đánh số thứ tự
Xuất hiện khí mùi khai và kết tủa trắng là dung dịch (NH4)2SO4
(NH4)2SO4 + Ba(OH)2 → BaSO4 ↓ + 2NH3 ↑ + 2H2O
Xuất hiện khí mùi khai là dung dịch NH4Cl
2NH4Cl + Ba(OH)2 → BaCl2 + 2NH3 ↑ + 2H2O
Xuất hiện kết tủa trắng → Na2SO4
K2SO4 + Ba(OH)2 → BaSO4↓ + 2NaOH
Không có hiện tượng là dung dịch NaCl
Câu 4. Amoniac phản ứng được với tất cả các chất trong nhóm nào sau đây (các điều kiện coi như có đủ)
A. HCl, O2, Cl2, dung dịch AlCl3
B. H2SO4, PbO, FeO, NaOH
C. HCl, NaOH, FeCl3, Cl2
D. NaOH, HNO3, CuO, CuCl2
Lời giải:
NH3 có tính bazơ nên không phản ứng được với bazơ mạnh
=>NaOH, KOH không phản ứng với NH3 loại B, C, D
Phương trình phản ứng
NH3 + HCl → NH4Cl
4NH3 + 5O2 → 4NO + 6H2O
8NH3 + 3Cl2 → N2 + 6NH4Cl
2NH3 + AlCl3 + 3H2O → Al(OH)3 ↓ + 3NH4Cl
Xem thêm các phương trình hóa học khác:
NH4Cl + NaOH → NH3 + H2O + NaCl
NH4Cl + Ca(OH)2 → CaCl2 + NH3 + H2O
NH4Cl + Ba(OH)2 → BaCl2 + NH3 + H2O
NH4Cl → NH3 + HCl
NH4NO3 → N2O + 2H2O
Cảm ơn bạn đã theo dõi bài viết tại Giải Bài Tập. Mời các bạn cùng xem các nội dung giải trí học tập và các kiến thức thú vị khác tại đây.




